题目内容
9.一定温度下,将 2mol SO2 和 1mol O2充入一定容密闭容器中,在催化剂存在下进行下列反应:2SO2(g)+O2(g)?2SO3(g)当达到平衡状态时,下列说法中正确的是( )| A. | 生成 SO3 为2mol | |
| B. | 单位时间消耗amol O2,同时消耗2amol SO2 | |
| C. | SO2 和 SO3物质的量之和一定为 2mol | |
| D. | SO2和SO3的浓度一定相等 |
分析 A.可逆反应的特点:反应不能进行到底.可逆反应无论进行多长时间,反应物都不可能100%地全部转化为生成物;
B.单位时间消耗amol O2,同时消耗2amol SO2都是指正反应方向;
C.根据元素守恒进行判断;
D.SO2的物质的量和SO3物质的量的大小关系取决于原始投料量和转化率.
解答 解:A.可逆反应无论进行多长时间,反应物都不可能100%地全部转化为生成物,故生成SO3小于2mol,故A错误;
B.单位时间消耗amol O2,同时消耗2amol SO2都是指正反应方向,故B错误;
C.根据S元素守恒可知,S的总的物质的量保持不变,即SO2和SO3物质的量之和一定为2mol,故C正确;
D.SO2的物质的量和SO3物质的量的大小关系取决于原始投料量和转化率,故D错误,
故选C.
点评 本题考查可逆反应的特点,难度不大,要注意可逆反应无论进行多长时间,反应物都不可能100%地全部转化为生成物.

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
20.下列有关实验的操作、原理和现象,正确的是( )
| A. | 取一定量酸性高锰酸钾溶液和过量草酸(H2C2O4)溶液混合,分成三等份,分别置于不同的温度下,观察比较溶液颜色变化的快慢以探究温度对反应速率的影响 | |
| B. | 可用酒精萃取溴水,将分液漏斗振摇几次后需要从分液漏斗上口放气 | |
| C. | 标准盐酸滴定待测NaOH溶液,水洗后的酸式滴定管未经标准液润洗,则测定结果偏低 | |
| D. | 用镊子夹取金属钠固体,切割取用后剩余的钠不能放回原试剂瓶中 |
17.已知下列三个反应:2Fe3++2I-═2Fe2++I2;2Fe2++Cl2═2Fe3++2Cl-;2MnO4-+10Cl-+16H+═2Mn2++5Cl2↑+8H2O,某溶液中有Fe2+、Cl-和I-,要氧化除去I-而又不影响Fe2+和Cl-,可加入的试剂是( )
| A. | Cl2 | B. | KMnO4 | C. | 浓HCl | D. | FeCl3 |
1.下列各组物质中分子数一定相同的是( )
| A. | 2gO3和2 gO2 | B. | 9克H2O和0.5NA个CO2 | ||
| C. | 标准状况下1molO2和22.4LH2O | D. | 0.2molH2和4.48LHCl |
18.(1)下表是元素周期表的一部分,针对表中的①~⑨种元素,填写下列空白:
在最高价氧化物的水化物中,酸性最强的化合物的分子式是HClO4,碱性最强的化合物的电子式是: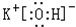 .
.
(2)在盛有500mL 0.1mol/LCuSO4溶液的大烧杯中.用锌、铜作电极,用导线连接形成原电池,写出电极反应式:负极Zn-2e-=Zn2+; 正极Cu2++2e-=Cu.
(3)过量的锌粉与一定量的稀盐酸反应,为了减慢反应速率,但是又不影响生成的氢气总量,可以采取的措施是B
A.升高温度 B.加入适量的水 C.加入少量CuSO4溶液 D.加入浓度较大的盐酸.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ |
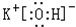 .
.(2)在盛有500mL 0.1mol/LCuSO4溶液的大烧杯中.用锌、铜作电极,用导线连接形成原电池,写出电极反应式:负极Zn-2e-=Zn2+; 正极Cu2++2e-=Cu.
(3)过量的锌粉与一定量的稀盐酸反应,为了减慢反应速率,但是又不影响生成的氢气总量,可以采取的措施是B
A.升高温度 B.加入适量的水 C.加入少量CuSO4溶液 D.加入浓度较大的盐酸.
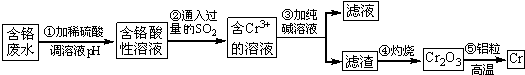
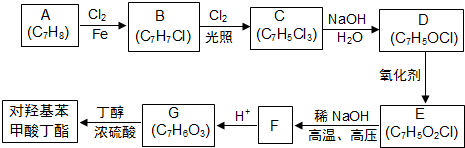
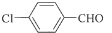 ; F的分子式为C7H4O3Na2;
; F的分子式为C7H4O3Na2;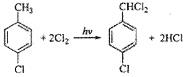 ,该反应类型为取代反应;
,该反应类型为取代反应;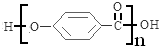 .
.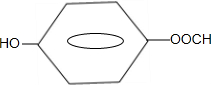 .
.