题目内容
20.下列有关实验的操作、原理和现象,正确的是( )| A. | 取一定量酸性高锰酸钾溶液和过量草酸(H2C2O4)溶液混合,分成三等份,分别置于不同的温度下,观察比较溶液颜色变化的快慢以探究温度对反应速率的影响 | |
| B. | 可用酒精萃取溴水,将分液漏斗振摇几次后需要从分液漏斗上口放气 | |
| C. | 标准盐酸滴定待测NaOH溶液,水洗后的酸式滴定管未经标准液润洗,则测定结果偏低 | |
| D. | 用镊子夹取金属钠固体,切割取用后剩余的钠不能放回原试剂瓶中 |
分析 A.应控制只有温度一个变量,探究温度对反应速率的影响;
B.酒精与水互溶;
C.水洗后的酸式滴定管应润洗;
D.钠易与空气中氧气和水反应,应保存在煤油中.
解答 解:A.因只有温度一个变量,则置于不同的温度下,观察比较溶液颜色变化的快慢以探究温度对反应速率的影响,故A正确;
B.酒精与水互溶,酒精不能萃取溴水中的溴,故B错误;
C.水洗后的酸式滴定管应润洗,否则未经标准液润洗,消耗标准液偏多,则测定结果偏高,故C错误;
D.做金属钠的性质实验时,剩余的钠放回原试剂瓶,由于钠很活泼,且如果将钠随意丢弃容易引起火灾、爆炸等事故,故D错误;
故选A.
点评 本题考查化学实验方案的评价,为高频考点,涉及反应速率影响因素、混合物分离提纯及实验操作等,把握反应原理及实验基本技能为解答的关键,侧重分析与实验能力的考查,题目难度不大.

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目
4.设NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 一定温度下,pH=6的纯水中含有OH-的数目为10-6NA | |
| B. | 120g NaHSO4固体中含有的离子总数为2NA | |
| C. | 标准状况下,22.4L乙烷中所含分子的数目为NA | |
| D. | 100mL 0.5mol/L-1的(NH4)2SO4溶液中,NH4+的数目为0.1NA |
11.甲醇是重要的化学工业基础原料和清洁液体燃料.工业上可利用CO或CO2来生产燃料甲醇.已知制备甲醇的有关化学反应以及在不同温度下的化学平衡常数如表所示:
(1)反应②是吸热(填“吸热”或“放热”)反应.
(2)某温度下反应①中H2的平衡转化率(a)与体系总压强(p)的关系如图甲所示.则平衡状态由A变到B时,平衡常数K(A)=K(B)(填“>”“<”或“=”).
(3)据反应①与②可推导出K1、K2与K3之间的关系,则K3=K1•K2(用K1、K2表示).500℃时测得反应③在某时刻时,H2(g)、CO2(g)、CH3OH(g)、H2O(g)的浓度(mol•L-1)分别为0.8、0.1、0.3、0.15,则此时v正>v逆(填“>”“=”或“<”).
(4)在3L容积可变的密闭容器中发生反应②,已知c(CO)-t(反应时间)变化曲线Ⅰ如图乙所示,若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ和曲线Ⅲ
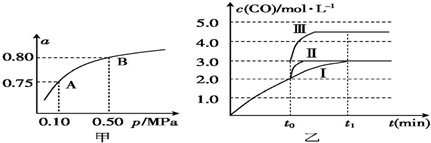
当曲线Ⅰ变为曲线Ⅱ时,改变的条件是加入催化剂
当曲线Ⅰ变为曲线Ⅲ时,改变的条是将容器的体积快速压缩至2L.
| 化学反应 | 平衡常温 | 温度(℃) | |
| 500 | 800 | ||
| ①2H2(g)+CO(g)?CH3OH(g) | K1 | 2.5 | 0.15 |
| ②H2(g)+CO2(g)?H2O(g)+CO(g) | K2 | 1.0 | 2.5 |
| ③3H2(g)+CO2(g)?CH3OH(g)+H2O(g) | K3 | ||
(2)某温度下反应①中H2的平衡转化率(a)与体系总压强(p)的关系如图甲所示.则平衡状态由A变到B时,平衡常数K(A)=K(B)(填“>”“<”或“=”).
(3)据反应①与②可推导出K1、K2与K3之间的关系,则K3=K1•K2(用K1、K2表示).500℃时测得反应③在某时刻时,H2(g)、CO2(g)、CH3OH(g)、H2O(g)的浓度(mol•L-1)分别为0.8、0.1、0.3、0.15,则此时v正>v逆(填“>”“=”或“<”).
(4)在3L容积可变的密闭容器中发生反应②,已知c(CO)-t(反应时间)变化曲线Ⅰ如图乙所示,若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ和曲线Ⅲ

当曲线Ⅰ变为曲线Ⅱ时,改变的条件是加入催化剂
当曲线Ⅰ变为曲线Ⅲ时,改变的条是将容器的体积快速压缩至2L.
8.根据所给下列4组物质,填写下表空白:
A.CuO、CO2、SO2、H2O B. Cl2、Na、Fe、Cu
C.HCl、HNO3、H2SO4、H2O D.Na2CO3、KCl、NaOH、AgNO3
A.CuO、CO2、SO2、H2O B. Cl2、Na、Fe、Cu
C.HCl、HNO3、H2SO4、H2O D.Na2CO3、KCl、NaOH、AgNO3
| A组 | B组 | C组 | D组 | |
| 分类标准 | 非金属氧化物 | 金属单质 | 酸 | 盐 |
| 不属于该类别的物质 | CuO | Cl2 | H2O | NaOH |
15.将2molA和1molB充入某密闭容器中发生反应:2A(g)+B(g)?xC(g),达到化学平衡后,C的体积分数为a,假设该反应的条件分别和下列各选项的条件相同,下列判断正确的是( )
| A. | 若在恒温恒压下:当x=1时,按1.5molA、1molC作为起始物质,达到平衡后,C的体积分数仍为a | |
| B. | 若在恒温恒容下:当x=2时,将3molC作为起始物质,达到平衡后,C的体积分数仍为a | |
| C. | 若在恒温恒压下:当x=3时,按1molA、1molB、1molC作为起始物质,达到平衡后,C的体积分数为a | |
| D. | 若在恒温恒容下:按0.6molA、0.3molB、1.4molC作为起始物质,达到平衡后,C的体积分数仍为a,则x为2或3 |
12.物质的提纯是化学实验中的一项重要操作,也是化工生产及物质制备中的主要环节.下列有关叙述中,正确的是( )
| A. | 除去乙烷中少量的乙烯,可将混合气体通入酸性高锰酸钾溶液 | |
| B. | 除去苯中含有的少量苯酚,可加入浓溴水过滤,即可除去苯酚 | |
| C. | 乙酸乙酯中混有乙酸,可用饱和Na2CO3溶液洗涤,然后分液分离出乙酸乙酯 | |
| D. | 在提纯鸡蛋中的蛋白质时,可向鸡蛋清溶液中加入浓CuSO4溶液,然后滤出沉淀,即得较纯的蛋白质 |
9.一定温度下,将 2mol SO2 和 1mol O2充入一定容密闭容器中,在催化剂存在下进行下列反应:2SO2(g)+O2(g)?2SO3(g)当达到平衡状态时,下列说法中正确的是( )
| A. | 生成 SO3 为2mol | |
| B. | 单位时间消耗amol O2,同时消耗2amol SO2 | |
| C. | SO2 和 SO3物质的量之和一定为 2mol | |
| D. | SO2和SO3的浓度一定相等 |
10.下列有机化合物分子中的所有碳原子不一定处于同一平面的是( )
| A. | 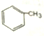 | B. | HC≡C-CH2-CH3 | C. | CH2=C(CH3)2 | D. | CH2=CHCH=CH2 |
 ,它是一种用途相当广泛的高分子聚合物.某研究小组设计的以乙烯为原料合成PVA的流程如图:
,它是一种用途相当广泛的高分子聚合物.某研究小组设计的以乙烯为原料合成PVA的流程如图:
 .
.