题目内容
9.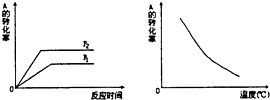 如图所示,可逆反应:mA(g)+nB(g)?xC(g),在不同温度、压强下反应物A的转化率的变化情况.下列对于反应的热效应和反应方程式中A、B、C的系数的判断中,正确的是( )
如图所示,可逆反应:mA(g)+nB(g)?xC(g),在不同温度、压强下反应物A的转化率的变化情况.下列对于反应的热效应和反应方程式中A、B、C的系数的判断中,正确的是( )| A. | 放热,m+n>x | B. | 放热,m+n<x | C. | 吸热,m+n<x | D. | 吸热,m+n>x |
分析 根据图(1)到达平衡时所用时间的长短判断压强p1和p2的相对大小,增大压强,化学平衡向气体体积减小的方向移动,由此判断反应前后气体化学计量数的相对大小;根据图(2)判断,升高温度,化学平衡向吸热方向移动,再结合A的转化率判断该反应的正反应是放热还是吸热.
解答 解:由图(1)知,p1到达平衡时所用时间长,p2到达平衡时所用时间短,根据“先拐先平数值大”可知则p2>p1;由图象知,压强越高,A的转化率增大,说明增大压强平衡向正反应方向移动,即正反应方向为气体体积减小的方向,所以反应前的计量数大于反应后的计量数,即m+n>x;
图(2)知,随着温度的升高,A的转化率减低,平衡向逆反应方向移动,升高温度,平衡向吸热反应方向移动,所以逆反应方向是吸热反应,正反应是放热反应,
故选A.
点评 本题考查化学平衡图象题,题目难度中等,注意温度、压强对反应速率和化学平衡的影响.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
20.已知:①Q、M、R、X、Y、Z为元素周期表中前四周期六种元素;②Q、M、X、Y为同周期原子序数依次增大的连续元素;③R、M、Z为同主族元素,下列判断正确的是( )
| A. | 这六种元素可能全部是主族元素 | B. | Y一定是主族元素 | ||
| C. | M与Z的原子核外电子数相差18 | D. | Q的最高价氧化物一定能溶于强碱 |
14. 乙醇分子中各化学键如图所示.下列关于乙醇在不同的反应中断裂化学键的说法错误的是( )
乙醇分子中各化学键如图所示.下列关于乙醇在不同的反应中断裂化学键的说法错误的是( )
 乙醇分子中各化学键如图所示.下列关于乙醇在不同的反应中断裂化学键的说法错误的是( )
乙醇分子中各化学键如图所示.下列关于乙醇在不同的反应中断裂化学键的说法错误的是( )| A. | 与金属钠反应时,键①断裂 | |
| B. | 在加热和Cu催化下与O2反应时,键①、③断裂 | |
| C. | 与浓硫酸共热发生消去反应时,键②③断裂 | |
| D. | 与乙酸、浓硫酸共热发生酯化反应时,键①断裂 |
1.氰酸铵(NH4OCN)与尿酸[CO(NH2)2]( )
| A. | 都是共价化合物 | B. | 都是离子化合物 | C. | 互为同素异形体 | D. | 互为同分异构体 |
18.下列有关金属的工业制法中,正确的是( )
| A. | 制铁:以铁矿石为原料,CO还原得铁 | |
| B. | 制钠:用海水为原料制得精盐,再电解纯净的NaCl溶液 | |
| C. | 制镁:用海水为原料,经一系列过程制得氧化镁固体,H2还原得镁 | |
| D. | 制铝:从铝土矿中获得氧化铝再得到氯化铝固体,电解熔融的氯化铝得到铝 |
 氯化铁是一种重要的铁盐,广泛用于造纸、印染等污染处理.某研究小组采用如图所示的装置制备少量纯净的氯化铁.
氯化铁是一种重要的铁盐,广泛用于造纸、印染等污染处理.某研究小组采用如图所示的装置制备少量纯净的氯化铁.