题目内容
14.二乙酸-1,4-环己二醇酯(G)是-种重要的有机化工原料,可通过下列路线合成:
(1)化合物E中含有的官能团的名称为羟基和碳碳双键.反应(步骤)④中所加入的试剂a为氢氧化钠水溶液.
(2)反应③可能生成的副产物为
 (写结构简式).
(写结构简式).在上述六步反应中,属于取代反应的是④⑤(填序号).
(3)写出同时满足下列条件的化合物H的一种同分异构体的结构简式:
 .
.I.分子式仅比F的少两个氧原子;Ⅱ.能与FeCl3溶液发生显色反应;
Ⅲ.分子中有2种不同化学环境的氢.
(4)请写出以CH2=CH-CH=CH2(1,3-丁二烯)、醋酸和醋酸酐为原料制备化合物
 的合成路线流程图(无机试剂任用).
的合成路线流程图(无机试剂任用).合成路线流程图示例如下:

分析 (1)根据E的结构简式可知其官能团,比较D和E的结构简式可知,反应④是将D中两个溴原子被羟基取代;
(2)C与溴可以发生1,4加成,也可以发生1,2加成或1,2,3,4加成;根据题中各物质转化关系可知,反应①为加成反应,反应②为消去反应,反应③为加成反应,反应④为取代反应,反应⑤为取代反应,反应⑥为加成反应;
(3)根据条件I.分子式仅比F的少两个氧原子;Ⅱ.能与FeCl3溶液发生显色反应,说明有酚羟基;Ⅲ.分子中有2种不同化学环境的氢,结合H的结构可写出符合条件的结构简式;
(4)以CH2=CH-CH=CH2(1,3-丁二烯)、醋酸和醋酸酐为原料制备化合物 ,可以先用与溴发生1,4加成,再水解得二元醇,再与乙酸酯化后发生加聚反应可得产品;
,可以先用与溴发生1,4加成,再水解得二元醇,再与乙酸酯化后发生加聚反应可得产品;
解答 解:(1)根据E的结构简式可知其官能团为羟基和碳碳双键,比较D和E的结构简式可知,反应④是将D中两个溴原子被羟基取代,所以反应中a试剂为氢氧化钠水溶液,
故答案为:羟基和碳碳双键;氢氧化钠水溶液;
(2)C与溴可以发生1,4加成,也可以发生1,2加成或1,2,3,4加成,生成产物为 ,根据题中各物质转化关系可知,反应①为加成反应,反应②为消去反应,反应③为加成反应,反应④为取代反应,反应⑤为取代反应,反应⑥为加成反应,
,根据题中各物质转化关系可知,反应①为加成反应,反应②为消去反应,反应③为加成反应,反应④为取代反应,反应⑤为取代反应,反应⑥为加成反应,
故答案为: ;④⑤;
;④⑤;
(3)根据条件I.分子式仅比F的少两个氧原子;Ⅱ.能与FeCl3溶液发生显色反应,说明有酚羟基;Ⅲ.分子中有2种不同化学环境的氢,结合H的结构可知,符合条件的结构简式为 ,
,
故答案为: ;
;
(4)以CH2=CH-CH=CH2(1,3-丁二烯)、醋酸和醋酸酐为原料制备化合物 ,可以先用与溴发生1,4加成,再水解得二元醇,再与乙酸酯化后发生加聚反应可得产品,合成的路线为
,可以先用与溴发生1,4加成,再水解得二元醇,再与乙酸酯化后发生加聚反应可得产品,合成的路线为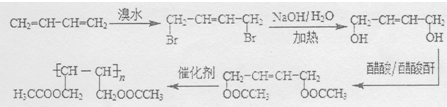 ,
,
故答案为: ;
;
点评 本题考查有机物的合成,题目难度不大,注意把握有机物的官能团与性质的关系即可解答,明确反应条件与反应类型的关系是解答的关键.

 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案| A. | 一定条件下,Cl2可在甲苯的苯环或侧链上发生取代反应 | |
| B. | 聚乙烯、聚乙炔都不能使酸性高锰酸钾褪色 | |
| C. | 乙烷和丙烯的物质的量共1mol,完全燃烧生成3molH2O | |
| D. | 光照下2,2-二甲基丙烷与Br2反应,其中一溴取代物只有一种 |
| A. | 为提高农作物的产量和质量,应大量使用化肥和农药 | |
| B. | 光缆在信息产业中有广泛应用,制造光缆的主要材料是单质硅 | |
| C. | 实现化石燃料清洁利用,就无需开发新能源 | |
| D. | 垃圾是放错地方的资源,应分类回收利用 |

| A. | M分子式为C6H6O7 | |
| B. | 1 mol物质M可以和3 mol氢气发生加成 | |
| C. | M分子不可以发生消除反应 | |
| D. | 足量的M分别与等物质的量的NaHCO3、Na2CO3反应得到的气体物质的量相同 |
| A. | 氯化氢溶于水 | B. | 加热氯酸钾使其分解 | ||
| C. | 干冰升华 | D. | 二氧化硅熔化 |
| A. | 乙烯、丙烯 | B. | 甲醇、乙二醇 | C. | 乙炔、苯 | D. | 丙烯、环丙烷 |
| A. | 氟化氢气体分解生成氢气和氟气的反应是放热反应 | |
| B. | 1 mol H2与1 mol F2反应生成2 mol液态HF放出的热量小于270 kJ | |
| C. | 在相同条件下,1 mol H2与1 mol F2的能量总和大于2 mol HF气体的能量 | |
| D. | 该反应中的能量变化可用如图来表示 |
| A. |  读数 | B. |  稀释 | C. |  称量 | D. |  溶解 |
| A. | X原子的最外层电子数和核电荷数肯定为奇数 | |
| B. | X能与某些金属元素形成化合物 | |
| C. | X能形成化学式为X(OH)3的碱 | |
| D. | X可能形成化学式为KXO3的盐 |