题目内容
18.在容积相同的两密闭容器A和B中,保持温度为423K,同时向A、B中分别加入a mol及b mol碘化氢(a>b),待反应2HI?I2(g)+H2(g)达平衡后,下列说法肯定正确的是( )| A. | 从反应开始到建立平衡所需时间:tA<tB | |
| B. | 平衡时I2的浓度:c(I2)A=c(I2)B | |
| C. | 平衡时碘蒸气在混合气体中的百分含量:A容器大于B容器 | |
| D. | 平衡时HI的分解率:αA=αB |
分析 容器A中反应物浓度大于容器B,但效果只是A中反应速率快,所需时间短,由于A容器中物质浓度大,故A的压强较大,增大压强反应向气体体积减小方向进行.但因为这个反应前后物质计量数之和都是2,所以不存在气体体积减小方向,平衡不移动,即压强对转化率没有影响,当平衡时A、B中HI的转化率是相同的.由于A中投料多,所以HI转化为更多的碘,体积相同,所以A容器中碘蒸气浓度更高.
解答 解:容器A中反应物浓度大于容器B,但效果只是A中反应速率快,所需时间短,由于A容器中物质浓度大,故A的压强较大,增大压强反应向气体体积减小方向进行.但因为这个反应前后物质计量数之和都是2,所以不存在气体体积减小方向,平衡不移动,即压强对转化率没有影响,当平衡时A、B中HI的转化率是相同的.由于A中投料多,所以HI转化为更多的碘,体积相同,所以A容器中碘蒸气浓度更高.
A、容器中A中反应物的浓度大,反应速率大,达平衡需要的时间少,t(A)<t(B)故A正确;
B、A容器中各物质的浓度比B容器中各物质的浓度大,故B错误.
C、平衡时A、B中HI的转化率相同,设转化率为x,平衡时A容器中:HI物质的量为a-ax,H2和I2均为$\frac{1}{2}$ax;平衡时B容器中:HI物质的量为b-bx,H2和I2为$\frac{1}{2}$bx,体积百分含量(也就是物质的量的百分含量)为$\frac{1}{2}$x,所以是相同的,故C错误;
D、两容器中平衡时HI的分解率相同,故D正确;
故选:AD.
点评 本题考查了反应前后气体体积不变的化学反应的等效平衡,在达到平衡时的各量的变化,化学平衡的计算,题目难度中等.

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案
相关题目
8.已知反应BeCl2+Na2BeO2+2H2O═2NaCl+2Be(OH)2↓能进行完全.以下推断中正确的是( )
| A. | BeCl2溶液pH<7,将其蒸干、灼烧后可得残留物BeCl2 | |
| B. | Na2BeO2溶液pH>7,将其蒸干、灼烧后可得残留物Na2BeO2 | |
| C. | Be(OH)2即能溶于盐酸,又能溶于NaOH溶液 | |
| D. | BeCl2水溶液的导电性强,BeCl2一定是离子晶体 |
9.某醇被氧化后的产物为酮(C5H10O),则该醇的结构简式可能是( )
| A. | (CH3)3CCH2OH | B. | (CH3CH2)2CHOH | C. | CH3(CH2)3CH2OH | D. | CH3CH2C(CH3)2OH |
13.A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大.A与D同主族;C与E同主族;B、C同周期;B原子最外层电子数比其次外层电子数多2;B、A两元素的核电荷数之差等于它们的原子最外层电子数之和;F元素是同周期元素中原子半径最小的主族元素.A、B、C、D、E、F形成的化合物甲、乙、丙、丁、戊、己的组成如下表所示.
回答下列问题:
(1)元素E在周期表中的位置第3周期第VIA族化合物丙的结构式为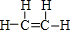 ,化合物甲的稳定性比戊高(填“高”或“低”) 化合物丁的化学键类型是离子键、共价键
,化合物甲的稳定性比戊高(填“高”或“低”) 化合物丁的化学键类型是离子键、共价键
(2)用电子式表示己的形成过程:
(3)单质B与浓硝酸发生化学反应的化学方程式为C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O
(4)向含有0.2mol乙的水溶液中加入少量MnO2,使乙完全反应,发生转移的电子数为0.2 NA(NA代表阿伏加德罗常数)
| 化合物 | 甲 | 乙 | 丙 | 丁 | 戊 | 己 |
| 化学式 | A2C | A2C2 | B2A4 | D2C2 | A2E | DF |
(1)元素E在周期表中的位置第3周期第VIA族化合物丙的结构式为
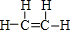 ,化合物甲的稳定性比戊高(填“高”或“低”) 化合物丁的化学键类型是离子键、共价键
,化合物甲的稳定性比戊高(填“高”或“低”) 化合物丁的化学键类型是离子键、共价键(2)用电子式表示己的形成过程:

(3)单质B与浓硝酸发生化学反应的化学方程式为C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O
(4)向含有0.2mol乙的水溶液中加入少量MnO2,使乙完全反应,发生转移的电子数为0.2 NA(NA代表阿伏加德罗常数)
3.在强碱性溶液中能大量共存且溶液为无色透明的离子组是( )
| A. | Na+、K+、SO42-、MnO4- | B. | Na+、NH4+、NO3-、Cl- | ||
| C. | K+、Ba2+、HCO3-、Cl- | D. | K+、Na+、CO32-、NO3- |
8.下列实验能达到预期目的是( )
| A. | 定性检验C2H5Cl中的氯元素:将C2H5Cl和NaOH溶液混合加热煮沸后,加AgNO3溶液 | |
| B. | 用碘酒验证汽油是否为裂化汽油 | |
| C. | 用鸡蛋清、硫酸铜、水完成蛋白质的变性实验 | |
| D. | 将无水乙醇加热到170℃制乙烯 |

