题目内容
【题目】往20ml1mol/L的AlCl3溶液中滴加0.2mol/L的NaOH溶液,最后有1.17克沉淀生成,则加入NaOH溶液的体积是
A.125mLB.275mLC.325mLD.450mL
【答案】C
【解析】
20mL1mol/L的AlCl3溶液中氯化铝的物质的量=0.02L×1mol/L=0.02mol,若Al元素都转化为氢氧化铝沉淀,则氢氧化铝沉淀的质量=0.02mol×78g/mol=1.56g>1.17g,说明有两种情况:一为沉淀不完全,只生成Al(OH)3沉淀;另一种情况为沉淀部分溶解,既生成Al(OH)3沉淀,又生成NaAlO2。
n(Al(OH)3)=![]() =0.015mol,
=0.015mol,
①若碱不足,由Al3++3OH═Al(OH)3↓可知,
NaOH的物质的量为0.015mol×3=0.045mol,
加入NaOH溶液的体积为![]() =0.225L=225mL;
=0.225L=225mL;
②沉淀部分溶解,既生成Al(OH)3沉淀,又生成NaAlO2,则:
Al3++3OH═Al(OH)3↓
0.02mol0.06mol0.02mol
溶解的氢氧化铝为0.02mol0.015mol=0.005mol
Al(OH)3+OH═AlO2+2H2O
0.005mol 0.005mol
则消耗的碱的物质的量为0.06mol+0.005mol=0.065mol,
加入NaOH溶液的体积为![]() =0.325L=325mL;
=0.325L=325mL;
答案选C。

 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案【题目】经测定乙醇的分子式为C2H6O。由于有机物普遍存在同分异构现象,推测乙醇结构可能是下列两种之一:(I)CH3CH2OH(II)CH3OCH3。为测定其结构,应利用物质的特殊性进行定性、定量实验。现给出乙醇、钠、水及必要的仪器,请甲、乙、丙三位同学直接利用如图给定的装置进行实验,确定乙醇的结构。
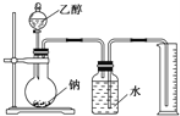
(1)学生甲得到一组实验数据:
乙醇的物质的量(mol) | 氢气的体积(标况)(L) |
0.10 | 1.13 |
0.10 | 1.11 |
0.10 | 1.12 |
0.10 | 1.18 |
请根据上表,帮助甲同学正确处理实验数据,氢气体积的平均值为__(L),由此推断乙醇的结构应为__式(用I或II表示),理由是___。写出乙醇与钠反应的化学方程式:___。
(2)同学乙分别准确称量4.60g乙醇进行多次实验,结果发现以排到量筒内的水的体积,作为生成的H2体积总是小于1.12L(换算成标准状况后)。如果忽略量筒本身及读数造成的误差,那么乙认为可能是由于样品中含有少量水造成的,你认为正确吗?___(填“正确”或“不正确”)。如果不正确,请说明理由:____。
(3)同学丙认为实验成功的关键有:①装置气密性要良好②实验开始前准确确定乙醇的量③钠足量④广口瓶内必须有足量水⑤氢气体积的测算方法正确、数值准确⑥应了解实验时的温度和大气压强。其中正确的有____。(填序号)