��Ŀ����
����Ŀ��ij��ѧС���Ա�����Ϊԭ�ϣ���ȡ�������������֪�й����ʵķе����±���
���� | �״� | ������ | ��������� | |
�е�/�� | 64.7 | 249 | 199.6 | |
�ܶ�/g.cm-3 | 0.792 | 1.2659 | 1.0888 | |
��.�ϳɱ���������ֲ�Ʒ
��Բ����ƿ�м���12.2 g�������20 mL�״�(�ܶ�ԼΪ0.79 g��cm��3)����С�ļ���3 mLŨ���ᣬ���Ⱥ�Ͷ�뼸�����Ƭ��С�ļ���ʹ��Ӧ��ȫ���ñ���������ֲ�Ʒ��
��1��Ũ�����������______________������Ӧ����ˮ��������ͬλ��18O��д���ܱ�ʾ��Ӧǰ��18Oλ�õĻ�ѧ����ʽ��_________________________________________��
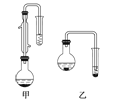
��2��������λͬѧ�ֱ��������ͼ��ʾ������ʵ���Һϳɱ����������װ��(�г������ͼ�������������ȥ)�������л���ķе㣬��ò���__________װ��(��ס����ҡ�)
��3����Ӧ��CH3OHӦ������������__________________________��
��.�ֲ�Ʒ�ľ���
��4������������ֲ�Ʒ���������������״����������ˮ�ȣ���������������ͼ���о��ƣ���������ͼ�з�����������������������ơ�

��5��ͨ�����㣬����������IJ���Ϊ__________��
���𰸡���1����������ˮ�� ![]() +CH3OH
+CH3OH![]()
![]()
��2���� ��3����Ӧ��CH3OH������ʹƽ�������ƶ�����������߱������ת����
��4����Һ������ ��5�� 65.0%
��������
�����������1��������Ӧ�У�Ũ����������Ǵ�������ˮ����������Ӧ�����������ǻ������⣬���Ի�ѧ����ʽΪ��![]() +CH3OH
+CH3OH![]()
![]() ��
��
��2������װ��ͼ��֪����ͼ�������ܣ�����������ã���ͼ��û�У��������з�Ӧ��״��е�ͣ������ᡢ����������ķе�Զ���ڼ״�����������ͼ���״��ض�������ӷ��������ںϳɷ�Ӧ�����Ը����л���ķе㣬��ò��ü�װ�á�
��3�����淴Ӧ�����в����ף�����һ�ַ�Ӧ��״���Ũ�ȣ�ʹƽ�����ƣ������������һ�ַ�Ӧ������ᣩ��ת���ʣ����Է�Ӧ��CH3OH�����������Ƿ�Ӧ��CH3OH������ʹƽ�������ƶ�����������߱������ת���ʡ�
��4������a����õ�ˮ����Ͳ㣬����a�Ƿ�Һ���л����ַ������ͬ���л������b�Ƿ���
��5�����������ݿ�֪�״���������������������㣬12.2g�ı���������ʵ�����0.1mol,������Ӧ�ñ����������������13.6g��ʵ�ʵ�8.84g�����Ա���������IJ���Ϊ8.84g/13.6g��100%=65.0%��