题目内容
【题目】【化学—选修5:有机化学】有机物A→F有如下转化关系: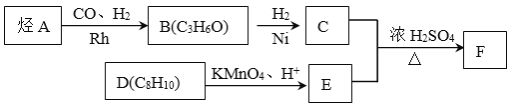
已知:①
②核磁共振氢谱显示C的分子中含有4种不同化学环境的氢原子,且峰面积之比为3:2:2:1。
③F是酯类化合物,分子中苯环上的一溴代物只有两种。
(1)A的分子式是 ,主要用途是 (写一种)。
(2)检验B中官能团的常用方法是 。
(3)D物质的名称为 。
(4)C+E→F的化学方程式是 。
(5)X与E互为同分异构体,且X有下列性质,符合条件的X有 种。
①接触NaHCO3有二氧化碳气体产生。
②与银氨溶液共热有银镜现象。
③1摩尔X与足量钠反应有1摩尔气体产生。
(6)Y与E也互为同分异构体,属于酯类化合物,分子中只含一种官能团,且苯环上的一硝基取代物只有一种,则Y的结构简式为 。
【答案】(1)C2H4 生产聚乙烯(或植物生长调节剂、果实催熟剂、工业制乙醇的原料)
(2)加入银氨溶液后,水浴加热一段时间,若看到有银镜生成,则证明有醛基(或加入新制氢氧化铜悬浊液,加热,若观察到砖红色沉淀生成,则证明有醛基)
(3)邻二甲苯(或1,2-二甲苯)
(4)![]() (3分)
(3分)
(5)10 (6)![]()
【解析】
试题分析:A发生已知信息①中的防御,根据生成物B的分子式可知A应该是乙烯,B是丙醛,结构简式为CH3CH2CHO。B与氢气发生加成反应生成C,则C是丙醇,结构简式为CH3CH2CH2OH。F是酯类化合物,这说明C和E发生的是酯化反应。又因为F分子中苯环上的一溴代物只有两种,所以D是邻二甲苯,被氧化生成邻二苯甲酸。
(1)根据以上分析可知乙烯的分子式是C2H4,主要用途是生产聚乙烯(或植物生长调节剂、果实催熟剂、工业制乙醇的原料)。
(2)B中含有醛基,则检验B中官能团的常用方法是加入银氨溶液后,水浴加热一段时间,若看到有银镜生成,则证明有醛基(或加入新制氢氧化铜悬浊液,加热,若观察到砖红色沉淀生成,则证明有醛基)。
(3)根据以上分析可知D物质的名称为邻二甲苯(或1,2-二甲苯)。
(4)根据以上分析可知C+E→F的化学方程式是![]() 。
。
(5)①接触NaHCO3有二氧化碳气体产生,说明含有羧基;②与银氨溶液共热有银镜现象,说明还含有醛基;③1摩尔X与足量钠反应有1摩尔气体产生,说明还含有羟基,则苯环上含有的取代基是-COOH、-OH、-CHO,其在苯环上的位置有10种。
(6)Y与E也互为同分异构体,属于酯类化合物,分子中只含一种官能团,且苯环上的一硝基取代物只有一种,则Y的结构简式为![]() 。
。

 阅读快车系列答案
阅读快车系列答案