题目内容
【题目】能源问题是人类社会面临的重大课题,甲醇是未来重要的绿色能源之一。
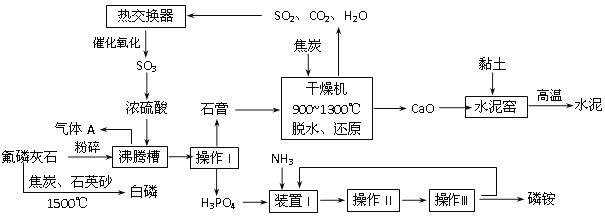
(1)利用工业废气CO2可制取甲醇,己知常温常压下下列反应的能量关系如图:

则CO2与H2反应生成液态CH3OH 的热化学方程式为_______________________。
(2)CH4 和H2O(g)通过下列转化也可以制得CH3OH:
I.CH4(g)+H2O(g)![]() CO(g)+3H2(g); △H1>0
CO(g)+3H2(g); △H1>0
II.CO(g)+2H2(g)![]() CH3OH(g); △H2<0
CH3OH(g); △H2<0
将1.0molCH4 和3.0molH2O (g)通入反应室(容积为100L)中,在一定条件下发生反应I,CH4的转化率与温度、压强的关系如下图所示。

① 图中的P1___P2(填“<”、“>”或“=”) ,判断的理由是________________。
② 若反应II在恒容密闭容器进行,下列能判断反应II达到平衡状态的是______(填序号)。
A.生成CH3OH 的速率与消耗CO 的速率相等 B.混合气体的密度不变
C.混合气体的总物质的量不变 D.CH3OH、CO、H2的浓度都不再发生变化
③在某温度下,将一定量的CO和H2投入10L的密闭容器中发生反应II,5min时达到平衡,各物质的物质的浓度(mol· L-1)变化如下表所示:
2min | 5min | 10min | |
CO | 0.07 | 0.06 | 0.05 |
H2 | 0.14 | 0.12 | 0.20 |
CH3OH | 0.03 | 0.04 | 0.05 |
若5min时只改变了某一条件,则所改变的条件是_______________。
【答案】(11分)(l)CO2(g)+3H2(g)=CH30H(l)+H2O(l) △H=-50kJ/mo1;(2)①<;该反应为反应前后气体体积增大的反应,温度相同时,压强越大,CH4的转化率越小,压强为P1的CH4的转化率高,所以P1<P2( 2 分);② c、d;③ 加了lmol氢气。
【解析】
试题分析:(1)图1中的热化学方程式为①CO(g)+H2O(l)=CO2(g)+H2(g) △H=-41kJ/mol,②CO(g)+ 2H2(g)=CH3 OH(l) △H= -(510-419)kJ/mol=-91KJ/mol,依据盖斯定律②-①得:二氧化碳和氢气制备甲醇的热化学方程式:CO2(g)+3H2(g)=CH30H(l)+H2O(l) △H=-50kJ/mo1;(2)将1.0mol CH4和2.0mol H2O(g)通入容积固定为100L的反应室,在一定条件下发生反应I,由图象可知T1℃甲烷转化率为50%,故参加反应的甲烷为1mol×50%=0.5mol,则:
CH4(g)+H2O(g) ![]() CO(g)+3H2(g); △H1>0
CO(g)+3H2(g); △H1>0
起始量(mol):1.0 3.0 0 0
变化量(mol):0.5 0.5 0.5 1.5
平衡量(mol):0.5 2.5 0.5 1.5
①该反应正方向为体积增大的方向,相同温度下,增大压强,甲烷的转化率减小,由图可知,相同温度下,P2的转化率比P1小,说明P1<P2;原因是该反应正方向为体积增大的方向,相同温度下,压强越大甲烷的转化率减小;② a.生成CH3OH的速率与消耗CO的速率均为正反应速率,不能判断平衡状态,错误;b.混合气体的体积始终保持不变,质量守恒,所以混合气体的密度始终不变,所以不能判断平衡状态,错误;c.该反应为气体的物质的量减少的反应,混合气体的总物质的量不变,说明反应达到平衡状态,正确;d.CH3OH、CO、H2的浓度都不再发生变化,说明反应达到平衡状态,正确;③反应达到平衡时,根据反应方程式知各物理量之间的关系式知,c(CO)=0.06mol/L,c(H2) =0.12mol/L,10min时,c(CO)减小,c(H2)增大,c(CH3OH)增大,则平衡向正反应方向移动,但氢气浓度增大,所以改变的物理量是增大了氢气的浓度,氢气浓度增大了0.2mol/L-0.12mol/L+0.02mol/L=0.1mol/L,则加入的氢气的物质的量为10L×0.1mol/L=1mol;即5min时只改变了某一条件,所改变的条件是增加1molH2。

 口算题天天练系列答案
口算题天天练系列答案