题目内容
已知热化学方程式:
① C2H2(g) +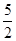 O2(g) == 2CO2(g)+H2O(l) ΔH1=-1301.0 kJ?mol-1
O2(g) == 2CO2(g)+H2O(l) ΔH1=-1301.0 kJ?mol-1
② C(s)+ O2(g) == CO2(g) △H2=-393.5 kJ?mol-1
③ H2(g)+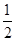 O2(g) == H2O(1) △H3 =" -285.8" kJ·mol-1
O2(g) == H2O(1) △H3 =" -285.8" kJ·mol-1
则反应④ 2C(s)+ H2(g) == C2H2(g)的△H为( )
① C2H2(g) +
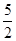 O2(g) == 2CO2(g)+H2O(l) ΔH1=-1301.0 kJ?mol-1
O2(g) == 2CO2(g)+H2O(l) ΔH1=-1301.0 kJ?mol-1② C(s)+ O2(g) == CO2(g) △H2=-393.5 kJ?mol-1
③ H2(g)+
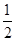 O2(g) == H2O(1) △H3 =" -285.8" kJ·mol-1
O2(g) == H2O(1) △H3 =" -285.8" kJ·mol-1则反应④ 2C(s)+ H2(g) == C2H2(g)的△H为( )
| A.+228.2 kJ·mol-1 | B.-228.2 kJ·mol-1 |
| C.+1301.0 kJ·mol-1 | D.+621.7 kJ·mol-1 |
A
试题分析:根据盖斯定律可知,②×2+③-①即得到反应④ 2C(s)+ H2(g) == C2H2(g),所以该反应的△H=-393.5 kJ?mol-1×2-285.8 kJ·mol-1+1301.0 kJ?mol-1=+228.2 kJ·mol-1,答案选A。
点评:根据热化学方程式计算反应热时,一般依据盖斯定律进行。

练习册系列答案
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案
相关题目
 CH3OCH3(g) + 3H2O(g) △H < 0
CH3OCH3(g) + 3H2O(g) △H < 0

 2NH3的能量变化下图所示,该反应的热化学方程式是 ( )
2NH3的能量变化下图所示,该反应的热化学方程式是 ( )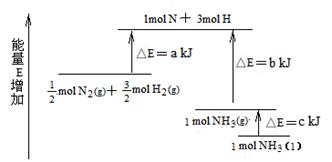
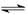 2NH3(1);△H=2(a-b-c)kJ·mol-1
2NH3(1);△H=2(a-b-c)kJ·mol-1 N2(g)+
N2(g)+ H2(g)
H2(g) 
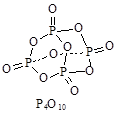
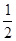 O2(g)=H2O(1)△H = ―285.8kJ/mol
O2(g)=H2O(1)△H = ―285.8kJ/mol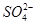 (aq)+Ba2+(aq)+2OH-(aq)===BaSO4(s)+2H2O(l) △H=-114.6 kJ·mol-1
(aq)+Ba2+(aq)+2OH-(aq)===BaSO4(s)+2H2O(l) △H=-114.6 kJ·mol-1 2NH3(g)△H="—38.6" kJ·mol—1
2NH3(g)△H="—38.6" kJ·mol—1