题目内容
3.在K2Cr2O7+14HCl→2KCl+2CrCl3+3Cl2+7H2O的反应中.(1)K2Cr2O7是氧化剂,HCl是还原剂,Cr被还原,Cl发生氧化反应,Cl2是氧化产物.
(2)标出电子转方向和数目;
(3)若有219g氯化氢被氧化,则生成氯气213g.
(4)若有219g氯化氢参加反应,则生成氯气91.3g.
分析 K2Cr2O7+14HCl→2KCl+2CrCl3+3Cl2+7H2O反应中Cr元素化合价降低,被还原,K2Cr2O7具有氧化性,Cl元素化合价升高,被氧化,HCl具有还原性,氧化还原反应中氧化剂和还原剂之间得失电子的数目相等,表现为化合价升降总数相等.
解答 解:(1)K2Cr2O7+14HCl→2KCl+2CrCl3+3Cl2+7H2O反应中Cr元素化合价降低,被还原,K2Cr2O7具有氧化性,为氧化剂,Cl元素的化合价升高,被氧化,则HCl具有还原性,作还原剂,生成的Cl2为氧化产物;
故答案为:K2Cr2O7;HCl;Cr;Cl;Cl2;
(2)元素化合价由+6价降低为+3价,化合价变化3价,Cl元素化合价升高1价,用单线桥法标出电子转移的方向和数目可表示为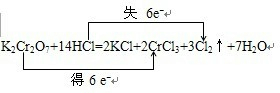 ,
,
故答案为: ;
;
(3)若有219g氯化氢被氧化,由氯原子守恒可知生成氯气为$\frac{219g×71}{36.5×2}$=213g;
故答案为:213;
(4)若有219g氯化氢参加反应,其中被氧化的HCl占总反应的$\frac{6}{14}$,则生成氯气为213g×$\frac{6}{14}$=91.3g;
故答案为:91.3.
点评 本题考查氧化还原反应知识,侧重于学生的分析能力的考查,题目难度不大,注意从元素化合价的角度判断氧化还原反应的相关概念,注意能熟练用单线桥法标出电子转移的方向和数目.

练习册系列答案
相关题目
13.下列反应中属于加成反应的是( )
| A. | 乙炔的燃烧 | B. | 苯的硝化反应 | ||
| C. | 乙烷跟氯气反应生成一氯乙烷 | D. | 乙烯与氯化氢作用生成一氯乙烷 |
14.下列有关化学用语使用正确的是( )
| A. | CH4分子的比例模型: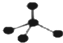 | B. | NH4Cl的电子式: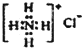 | ||
| C. | S2-结构示意图: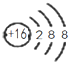 | D. | 聚丙烯的结构简式为: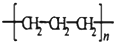 |
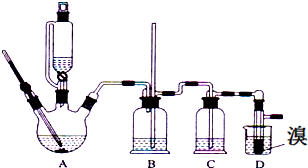
2.实验室用少量的溴和足量的乙醇、浓硫酸制备1,2-二溴乙烷的装置如图所示,其中可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚.
有关数据列表如下:
回答下列问题:
(1)用少量的溴和足量的乙醇、浓硫酸制备1,2-二溴乙烷的两步反应方程式为:CH3CH2OH $→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O;CH2=CH2+Br-Br→CH2Br-CH2Br
(2)装置B中玻璃管的作用控制气体流速,防止危险
(3)装置C中加入氢氧化钠溶液,其目的是吸收反应中生成的SO2、CO2气体 (填分子式)
(4)反应过程中应用冷水冷却装置D,其主要目的是避免溴大量挥发;但又不能过度冷却(如用冰水),其原因是产品1,2-二溴乙烷的熔点(凝固点)低,过度冷却会凝固而堵塞导管.
(5)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在下层(填“上”、“下”);
(6)若产物中有少量未反应的Br2,最好用NaOH溶液试剂除去;
(7)若产物中有少量副产物乙醚.可用蒸馏方法除去.

有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | 一l30 | 9 | -1l6 |
(1)用少量的溴和足量的乙醇、浓硫酸制备1,2-二溴乙烷的两步反应方程式为:CH3CH2OH $→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O;CH2=CH2+Br-Br→CH2Br-CH2Br
(2)装置B中玻璃管的作用控制气体流速,防止危险
(3)装置C中加入氢氧化钠溶液,其目的是吸收反应中生成的SO2、CO2气体 (填分子式)
(4)反应过程中应用冷水冷却装置D,其主要目的是避免溴大量挥发;但又不能过度冷却(如用冰水),其原因是产品1,2-二溴乙烷的熔点(凝固点)低,过度冷却会凝固而堵塞导管.
(5)将1,2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在下层(填“上”、“下”);
(6)若产物中有少量未反应的Br2,最好用NaOH溶液试剂除去;
(7)若产物中有少量副产物乙醚.可用蒸馏方法除去.
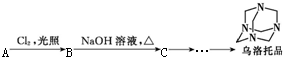

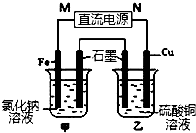 如图装置中甲烧杯盛放100mL 0.2mol/L的NaCl溶液,乙烧杯盛放100 mL 0.5mol/L的CuSO4溶液.向甲烧杯中滴入几滴酚酞,反应一段时间后,观察到石墨电极附近首先变红,乙烧杯中石墨电极附近pH值的变化为变小(选填“变大”、“变小”、“不变”).通电一段时间后(溶液中还有CuSO4),停止通电.若要使乙烧杯中电解质溶液恢复到电解前的状态,可加入AC (填序号).
如图装置中甲烧杯盛放100mL 0.2mol/L的NaCl溶液,乙烧杯盛放100 mL 0.5mol/L的CuSO4溶液.向甲烧杯中滴入几滴酚酞,反应一段时间后,观察到石墨电极附近首先变红,乙烧杯中石墨电极附近pH值的变化为变小(选填“变大”、“变小”、“不变”).通电一段时间后(溶液中还有CuSO4),停止通电.若要使乙烧杯中电解质溶液恢复到电解前的状态,可加入AC (填序号).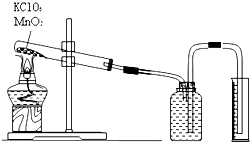 某小组设计利用氯酸钾制氧气来测定气体摩尔体积的探究实验.装置
某小组设计利用氯酸钾制氧气来测定气体摩尔体积的探究实验.装置