题目内容
12.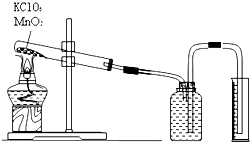 某小组设计利用氯酸钾制氧气来测定气体摩尔体积的探究实验.装置
某小组设计利用氯酸钾制氧气来测定气体摩尔体积的探究实验.装置实验步骤如下:
①将适量的氯酸钾粉末和二氧化锰粉末混合均匀,放入干燥的试管中,准确称量试管和药品的总质量为15.95g.
②连接好实验装置,检查装置的气密性.
③加热反应,直到不再有气体产生为止.
④测量排入量筒的水的体积为285.0mL.
⑤准确称量试管和残留物的质量为15.55g.
根据上述实验过程,回答下列问题:
(1)此装置如何检查气密性往广口瓶中注满水,塞紧橡皮塞,按装置图连接好装置,用手将试管底部捂热,若观察到广口瓶中长玻璃管内液面上升,松开手后,过一会长玻璃管内的液面下降,则证明该装置不漏气
(2)本实验通过读取量筒内水的体积来测得收集的气体的体积,但在此操作前还需进行两步主要操作,请按操作顺序写出:
①使气体都冷却至室温;②调整量筒内外液面高度使之相同;读取量筒内气体的体积;仰视读数使得读数偏小.
读取量筒内液体体积时,若俯视读数,则读取的氧气的体积偏大(选填“偏大”、“偏小”、“无影响”).
(3)实验中产生的氧气的物质的量是0.0125 mol;实验测得的氧气的气体摩尔体积是22.8L/mol(精确到0.01)
分析 (1)装置气密性检验的原理是:通过气体发生器与附设的液体构成封闭体系,依据改变体系内压强时产生的现象(如气泡的生成、水柱的形成、液面的升降等)来判断装置气密性;
(2)要准确测量气体体积必须保持量筒内外气体的温度和压强相等,因此在读取量筒内气体的体积之前,应使试管和量筒内的气体都冷却至室温;再调节量筒内外液面高度使之相同;仰视量筒,是刻度定液面,量取体积增大;
(3)试管和药品在实验前后的质量差即为生成的氧气的质量,根据气体摩尔体Vm=$\frac{V}{n}$计算.
解答 解:(1)装置气密性检验的原理是:通过气体发生器与附设的液体构成封闭体系,依据改变体系内压强时产生的现象(如气泡的生成、水柱的形成、液面的升降等)来判断装置气密性.加热高锰酸钾制取氧气时的检验装置气密性的方法为:往广口瓶中注满水,塞紧橡皮塞,按装置图连接好装置,用手将试管底部捂热,若观察到广口瓶中长玻璃管内液面上升,松开手后,过一会长玻璃管内的液面下降,则证明该装置不漏气;
故答案为:往广口瓶中注满水,塞紧橡皮塞,按装置图连接好装置,用手将试管底部捂热,若观察到广口瓶中长玻璃管内液面上升,松开手后,过一会长玻璃管内的液面下降,则证明该装置不漏气;
(2)因为排出的气体是需要用排出的水的体积衡量的,而反应前后的量筒温度是不同的,因此,反应终止应该先停止加热,待体系恢复到室温时,才取出导管.这一步操作跟通常的实验不同,所以停止加热时导管的出口要高于量筒内的液面,此时即使不取出导管而停止加热,也不会造成水的倒吸;停止加热、回到室温后,将量筒下移以调节量筒内的液面与水槽一致,此时量筒内气体压强也为大气压,读数才是正确的;所以正确的操作顺序为:使试管和广口瓶内气体都冷却至室温;调整量筒的高度使其液面与广口瓶内液面相平;读取量筒内气体的体积;仰视读数使得量取液体体积大于刻度线,量取结果偏大,
故答案为:使试管和广口瓶内气体都冷却至室温;调整量筒的高度使其液面与广口瓶内液面相平;偏大;
(3)生成的氧气的质量m=15.95g-15.55g=0.4g,氧气物质的量n=$\frac{m}{M}$=$\frac{0.4g}{32g/mol}$=0.0125mol,氧气的体积v=285mL=0.285L.则气体摩尔体积Vm=$\frac{V}{n}$=$\frac{0.285L}{0.0125mol}$=22.8L/mol.
故答案为:0.0125mol;22.8L/mol.
点评 本题比较全面的考查了化学实验双基知识,包括的考点有实验的操作、原理、数据的采用和处理,考察对装置图形的观察,利用常用的中学仪器做定量实验,难度中等.

| A. | 常温常压下,1 mol Fe与足量稀HNO3反应,转移电子数目一定为为3NA | |
| B. | 0.1 mol/L NaHCO3溶液中含有Na+数目为0.1NA | |
| C. | 50mL 18.4mol/L浓硫酸与足量铜微热反应,生成SO2分子数目为0.46NA | |
| D. | 常温下,1 mol Fe与足量浓硫酸反应,转移电子数目一定为为3NA |
| A. | 碘的升华 | B. | 生石灰溶于水 | C. | 镁与稀盐酸反应 | D. | 氨气分解 |
| A. | 4:5 | B. | 1:1 | C. | 1:5 | D. | 4:1 |
| A. | 通入HCl气体 | B. | 加入适量氢氧化钠固体 | ||
| C. | 加入适量KHCO3 | D. | 加入适量Na2CO3晶体 |
| A. | FeS2$\stackrel{O_{2}/高温}{→}$SO2$\stackrel{H_{2}O_{2}(aq)}{→}$H2SO4 | |
| B. | 饱和NaCl溶液$\stackrel{NH_{3},CO_{2}}{→}$NaHCO3$\stackrel{△}{→}$Na2CO3 | |
| C. | CuSO4(aq)$\stackrel{过量NaOH(aq)}{→}$Cu(OH)2$\stackrel{葡萄糖(aq)/△}{→}$Cu2O | |
| D. | 1 mol•L-1HCl(aq)$\stackrel{MnO_{2}/△}{→}$Cl2$\stackrel{石灰乳}{→}$Ca(ClO)2 |
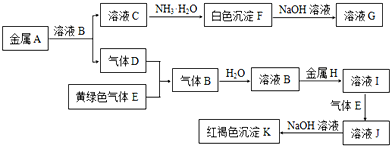
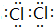 ,G的化学式是NaAlO2.
,G的化学式是NaAlO2.