题目内容
20.下列说法正确的是( )| A. | 稀有气体元素最外层电子数均为8个 | |
| B. | 原子最外层少于4个电子的元素均是金属元素 | |
| C. | 相同条件下,H2O的沸点比H2S高是因为水分子间含有氢键 | |
| D. | 目前人们已发现了5000多种核素,说明发现了5000多种元素 |
分析 A.氦最外层2个电子;
B.原子最外层少于4个电子的元素不一定是金属元素,例如:H、He等;
C.水分子间存在氢键;
D.同一元素存在多种核素.
解答 解:A.He元素原子核外只有2个电子,其余稀有气体原子最外层电子数均为8,故A错误;
B.原子最外层少于4个电子的元素不一定是金属元素,例如:H、He等,故B错误;
C.水分子间存在氢键,所以H2O的沸点比H2S高,故C正确;
D.目前只发现100多种元素,同一元素存在多种核素,核素种数远远大于元素种数,故D错误,
故选C.
点评 本题考查特殊元素原子结构特点、核素等,比较基础,侧重对基础知识的巩固.

练习册系列答案
相关题目
10.下列比较正确的是( )
| A. | 酸性:H2CO3>H2SiO3>H3PO4 | B. | 碱性:CsOH>Ba(OH)2>Ca(OH)2 | ||
| C. | 热稳定性:H2O>HF>NH3>HCl | D. | 氧化性:Ag+<Cu2+<H+<Fe2+ |
8.下列化合物分子中只含σ键不含π键的是( )
| A. | CO2 | B. | COCl2 | C. | C2H2 | D. | H2O2 |
15.如果发现了原子序数为116的元素,对它的正确叙述是下列组合中的( )
①位于第七周期 ②是非金属元素 ③最外电子层含有6个电子
④没有放射性 ⑤属于ⅥA族元素 ⑥属于ⅦA族元素.
①位于第七周期 ②是非金属元素 ③最外电子层含有6个电子
④没有放射性 ⑤属于ⅥA族元素 ⑥属于ⅦA族元素.
| A. | ①③⑤ | B. | ①③⑥ | C. | ②④⑥ | D. | ②③⑤ |
5. 把镁条投入到盛有稀硫酸的敞口容器中,产生H2的速率如图所示,在下列因素中,①H+的浓度 ②镁条的表面积 ③溶液的温度 ④SO42-的浓度,影响反应速率的因素是( )
把镁条投入到盛有稀硫酸的敞口容器中,产生H2的速率如图所示,在下列因素中,①H+的浓度 ②镁条的表面积 ③溶液的温度 ④SO42-的浓度,影响反应速率的因素是( )
 把镁条投入到盛有稀硫酸的敞口容器中,产生H2的速率如图所示,在下列因素中,①H+的浓度 ②镁条的表面积 ③溶液的温度 ④SO42-的浓度,影响反应速率的因素是( )
把镁条投入到盛有稀硫酸的敞口容器中,产生H2的速率如图所示,在下列因素中,①H+的浓度 ②镁条的表面积 ③溶液的温度 ④SO42-的浓度,影响反应速率的因素是( )| A. | ①④ | B. | ①②③ | C. | ②③ | D. | ③④ |
12.已知钍(${\;}_{90}^{232}$Th)的原子可发生下列放射性变化,${\;}_{90}^{232}$Th→${\;}_{88}^{228}$X+${\;}_{2}^{4}$α,生成的X是与钫(Fr)同周期的一种元素的原子,下列对X的推断错误的是( )
| A. | X的氢氧化物是一种强碱 | B. | X的碳酸正盐不溶于水 | ||
| C. | X原子核外有6个电子层 | D. | X的最高化合价为+2价 |
10.石墨和金刚石都是碳的单质,石墨在一定条件下可转化为金刚石.已知把石墨完全转化为金刚石时,要吸收能量,下列说法正确的是( )
| A. | 等质量的金刚石与石墨完全燃烧,放出的能量一样多 | |
| B. | 等质量的金刚石与石墨完全燃烧,石墨放出的能量少 | |
| C. | 石墨不如金刚石稳定 | |
| D. | 金刚石不如石墨稳定 |

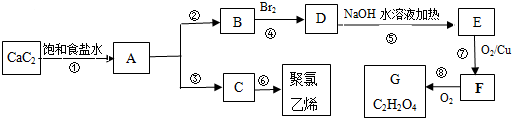
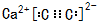 ,A的结构式H-C≡C-H,B分子中碳原子的杂化方式是sp2
,A的结构式H-C≡C-H,B分子中碳原子的杂化方式是sp2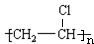 .
.