题目内容
5.2010年诺贝尔物理奖授予发现石墨烯的开创性研究者,金刚石、石墨、C60和石墨烯的结构示意图分别如下图所示,下列说法不正确的是( )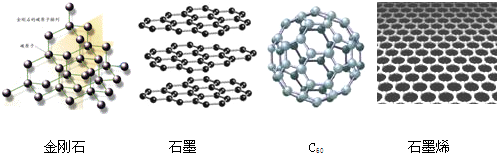
| A. | 金刚石和石墨烯中碳原子的杂化方式不同 | |
| B. | 金刚石、石墨、C60 和石墨烯的关系:互为同素异形体 | |
| C. | 这四种物质完全燃烧后的产物都是CO2 | |
| D. | 石墨与C60的晶体类型相同 |
分析 A.根据价层电子对互斥理论确定其杂化类型;
B.同素异形体是相同元素组成的不同形态的单质;
C.碳和氧气反应生成二氧化碳;
D.石墨与C60的晶体类型不相同,前者是混合晶体,后者是分子晶体.
解答 解:A.金刚石中每个碳原子和4个碳原子以σ键相结合,且没有孤对电子,所以每个 碳原子的价层电子对是4,则碳原子采取sp3杂化,石墨烯中每个C原子价层电子对个数是3,根据价层电子对互斥理论知C原子杂化类型为sp2,故A正确;
B.金刚石、石墨、C60 和石墨烯都是碳元素组成的单质,属于同素异形体,故B正确;
C.金刚石、石墨、C60 和石墨烯都是碳元素组成的单质,碳和氧气反应生成二氧化碳,故C正确;
D.石墨为原子晶体结构和分子晶体结构兼有的混合晶体,C60为分子晶体,故D错误;
故选D.
点评 本题主要考查了金刚石、石墨、C60和石墨烯的结构,掌握常见晶体的结构是解答的关键,题目难度中等.

练习册系列答案
相关题目
15.下列说法正确的是( )
| A. | pH=2与pH=1的硝酸中c(H+)之比为1:10 | |
| B. | Na2CO3溶液中c(Na+)与c(CO32-)之比为2:1 | |
| C. | 0.2 mol•L-1与0.1mol/L醋酸中c (H+)之比为2:1 | |
| D. | NO2溶于水时,被氧化的n(NO2)与被还原的n(NO2)之比为3:1 |
16.一块质量为4g的合金,与足量的盐酸反应完全后生成氢气0.2g,则该合金可能是( )
| A. | 铁镁合金 | B. | 铁铜合金 | C. | 铁锌合金 | D. | 镁铝合金 |
13.下列说法不正确的是( )
| A. | 增大反应物浓度,可增大单位体积内活化分子数,从而使反应速率增大 | |
| B. | 有气体参加的化学反应,若增大压强(即缩小反应容器体积),可增加单位体积内活化分子数,从而使反应速率增大 | |
| C. | 活化分子间所发生的碰撞为有效碰撞 | |
| D. | 升高温度能使化学反应速率增大的主要原因是增加了反应物中活化分子数 |
10.下列说法不正确的是( )
| A. | 用价层电子对互斥理论预测H2S和BF3的立体结构为:V形和平面三角形 | |
| B. | 分子晶体中一定存在分子间作用力,不一定存在共价键 | |
| C. | SiO2晶体中每个硅原子与两个氧原子以共价键相结合 | |
| D. | CCl2F2无同分异构体,说明其中碳原子采用sp3方式杂化 |
17.化学已渗透到人类生活的各个方面.下列说法正确的是( )
| A. | 食盐加碘和酱油加铁是为了补存人体所需要的常量元素 | |
| B. | 瘦肉精能提高猪肉的瘦肉率,食用含瘦肉精的猪肉,不会对人体造成危害 | |
| C. | 日本核泄漏事故释放出放射性核素碘-131,极微量碘-131不会对人体产生危害 | |
| D. | 高纯度的硅单质广泛用于制作光导纤维 |
12.下列各对物质中,互为同系物的是( )
| A. | CH3-CH2-CH3和 CH3-CH=CH2 | B. | CH3-CH=CH2和 CH3-CH2-CH=CH2 | ||
| C. | CH3-CH3和 CH3-CH=CH2 | D. | CH2=CH2和 CH≡CH |
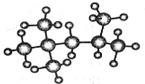 (1)在有机物:①CH3CH3、②CH2=CH2、③CH3CH2C≡CH、④CH3C≡CCH3、
(1)在有机物:①CH3CH3、②CH2=CH2、③CH3CH2C≡CH、④CH3C≡CCH3、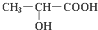 .对于人的身体来说,乳酸是疲劳物质之一,是身体在保持体温和肌体运动而产生热量过程中产生的废弃物.试回答:
.对于人的身体来说,乳酸是疲劳物质之一,是身体在保持体温和肌体运动而产生热量过程中产生的废弃物.试回答: +2Na→
+2Na→ +H2↑,.
+H2↑,.