题目内容
20.(1)Al2(SO4)3的水溶液呈酸(填“酸”、“中”、“碱”)性,常温时的pH<7(填“>”、“=”、“<”),原因是(用离子方程式表示):Al3++3H2O?Al(OH)3+3H+;实验室在配制Fe2(SO4)3的溶液时,常将Fe2(SO4)3固体先溶于较浓的(化学式)H2SO4中,然后再用蒸馏水稀释到所需的浓度,以抑制(填“促进”、“抑制”)其水解.(2)在配制硫化钾(K2S)溶液时,为了防止发生水解,可以加入少量的KOH.
分析 (1)硫酸铝是强酸弱碱盐,铝离子水解导致溶液呈酸性,溶液PH小于7,要抑制铝离子水解,配制Fe2(SO4)3的溶液时可以在较浓的硫酸溶液中稀释得到;
(2)在配制硫化钾(K2S)溶液时,硫离子水解溶液显碱性,为了防止发生水解,应加入对应碱;
解答 解:(1)硫酸铝是强酸弱碱盐,铝离子水解导致溶液呈酸性,常温时的pH<7,水解方程式为Al3++3H2O?Al(OH)3+3H+,实验室在配制Fe2(SO4)3的溶液时,要抑制铁离子水解且不引进新的杂质离子,常将Fe2(SO4)3固体先溶于较浓的硫酸,然后再用蒸馏水稀释到所需的浓度,抑制其水解,
故答案为:酸,<,Al3++3H2O?Al(OH)3+3H+,H2SO4,抑制;
(2)在配制硫化钾(K2S)溶液时,硫离子水解溶液显碱性,为了防止发生水解,应加入对应碱,可以加入少量的氢氧化钾,
故答案为:KOH;
点评 本题考查了盐类水解,根据盐的类型结合“谁强谁显性、谁弱谁水解”确定溶液酸碱性,难点是离子方程式的书写,题目难度不大.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
10.下列各原子或离子的电子排布式错误的是( )
| A. | Ca2+ 1s22s22p63s23p6 | B. | O2-1s22s23p4 | ||
| C. | Cl- 1s22s22p63s23p6 | D. | Ar 1s22s22p63s23p6 |
11.如图实验不能达到目的是( )
| A. | 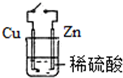 原电池能加快反应速率 | B. | 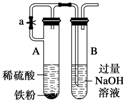 制备Fe(OH)2 | ||
| C. | 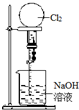 喷泉实验 | D. | 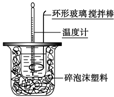 中和热的测定 |
8.许多城市都限制燃放烟花爆竹,除噪声污染外,爆竹燃放时会产生一种无色有刺激性气味、有毒的气体,这种气体是( )
| A. | N2 | B. | SO2 | C. | CO2 | D. | C12 |
15.家庭居室装潢后,室内产生污染的有机气体是( )
| A. | SO2 | B. | CO | C. | HCHO | D. | NO |
5.2010年诺贝尔物理奖授予发现石墨烯的开创性研究者,金刚石、石墨、C60和石墨烯的结构示意图分别如下图所示,下列说法不正确的是( )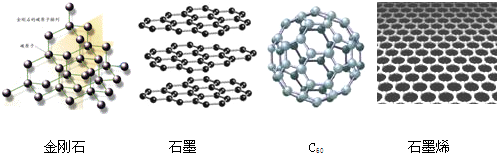

| A. | 金刚石和石墨烯中碳原子的杂化方式不同 | |
| B. | 金刚石、石墨、C60 和石墨烯的关系:互为同素异形体 | |
| C. | 这四种物质完全燃烧后的产物都是CO2 | |
| D. | 石墨与C60的晶体类型相同 |
7.两种气态烃混合气体共1L,在空气中完全燃烧得到1.5L CO2和2.5L水蒸气(气体体积均在150℃条件下测定),关于此混合气体的判断合理的是( )
| A. | 一定含有甲烷 | B. | 一定有乙烷 | ||
| C. | 可能是乙烷和甲烷的混合气体 | D. | 可能是甲烷和丙烯(C3H6)的混合气体 |
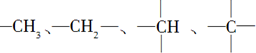 中的碳原子分别称为伯、仲、叔、季碳原子,数目分别用N1、N2、N3、N4表示.例如:
中的碳原子分别称为伯、仲、叔、季碳原子,数目分别用N1、N2、N3、N4表示.例如: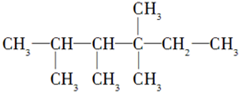
 ;E3+的离子符号为Fe3+.
;E3+的离子符号为Fe3+.