题目内容
18.与下列装置相关的说法中不正确的是( )| A. | 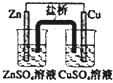 如装置中,盐桥中的K+移向CuSO4溶液 | |
| B. | 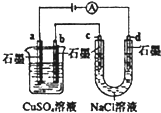 如图装置中b极析出6.4g固体时,d极产生2.24LH2 | |
| C. | 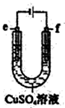 用如图装置精炼铜时,f极为粗铜 | |
| D. | 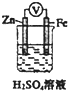 如图装置中电子沿导线由Zn流向Fe,Fe极上有大量气泡生成 |
分析 A.含有盐桥的原电池放电时,盐桥中的阳离子向正极移动;
B.根据串联电解池中转移电子数相等计算;
C.电解精炼时,粗铜作阳极,纯铜作阴极;
D.原电池放电时,正极上得电子发生还原反应.
解答 解:A.该原电池中,锌作负极,铜作正极,原电池放电时,盐桥中的钾离子向硫酸铜溶液移动,故A正确;
B.该串联电解池中,b极、d极都是阴极,b极上析出铜,d极上析出氢气,根据转移电子数相等知,铜和氢气的关系式是Cu~H2,析出6.4g铜时,生成0.1mol氢气,但温度和压强未知,所以气体摩尔未知,无法确定氢气体积大小,故B错误;
C.电解精炼时,粗铜作阳极,所以f极为粗铜,故C正确;
D.该装置是原电池,锌作负极,铁作正极,有大量气泡生成,放电时,电子从锌极沿导线流向铁极,故D正确;
故选B.
点评 本题考查原电池和电解池原理,明确离子的放电顺序、及电极反应即可分析解答,易错选项是B,气体体积的计算要注意温度和压强,为易错点.

练习册系列答案
 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
6.根据下列实验及现象,能量关系正确的是( )
| 实验及现象 | 能量关系 | |
| A | 将“NO2球”置于热水中,红棕色加深 | N2O4(g)?2NO2(g)△H<0 |
| B | NaOH与HCl溶液混合,溶液温度升高 |  |
| C | 钠投入水中,熔化成小球 |  |
| D | 微热含酚酞的Na2CO3溶液,红色加深 | CO32-(aq)+H2O(l)?HCO3-(aq)+OH-(aq)△H<0 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
13.如图所示,甲池的总反应式为N2H4+O2=N2+2H2O,.下列说法正确的是( )
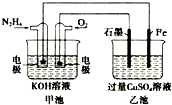

| A. | 甲池中负极上的电极反应式为N2H4-4e-=N2+4H+ | |
| B. | 乙池中石墨电极上发生的反应为4OH--4e-=2H2O+O2↑ | |
| C. | 甲池溶液pH增大,乙池溶液pH减小 | |
| D. | 甲池中每消耗0.1mol N2H4乙池电极上则会析出6.4g固体 |
3.已知金刚石的燃烧热为395kJ/mol,下表是部分化学键的键能数据.下列选项中正确的是( )
| 化学键 | C-C | O=O | C=O |
| 键能(kJ/mol) | 348 | 498 | x |
| A. | x=794.5 | |
| B. | x=1142.5 | |
| C. | 1mol金刚石的能量一定比1mol CO2能量高 | |
| D. | 金刚石燃烧的热化学方程式为 2C(s)+O2(g)=2CO(g)△H=-790 kJ/mol |
10.元素周期表与元素周期律在学习、研究和生产实践中有很重要的作用.下表列出了①~⑨九种元素在周期表中的位置.请回答:
(1)编号元素中,化学性质最不活泼元素的原子结构示意图是Ne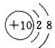 .
.
(2)九种元素中非金属性最强的是F(填元素符号),元素⑧的氢化物的电子式为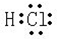 ,
,
(3)除⑨外,原子半径最大的是Na(填元素符号).在①、②、③三种元素的最高价氧化物对应的水化物中,碱性最强的是NaOH(填化学式).电子式为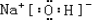 ,所含有的化学键类型有离子键、极性共价键,(请选择“离子键”、“极性共价键”、“非极性共价键”中的一个或几个填写).
,所含有的化学键类型有离子键、极性共价键,(请选择“离子键”、“极性共价键”、“非极性共价键”中的一个或几个填写).
(4)⑥⑦⑧三种元素的气态氢化物的稳定性由强到弱的顺序是HF>HCl>H2S.(用相应的氢化物的化学式作答)
(5)元素④对应的氢化物的化学式是NH3,电子式为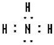 ,其水溶液的pH>7(填“<”或“>”).
,其水溶液的pH>7(填“<”或“>”).
(6)⑦⑧两种元素对应的最高价含氧酸的酸性由强到弱的顺序是HClO4>H2SO4.(用相应的最高价氧化物对应水化物的化学式作答)
(7)①的阳离子与⑥的阴离子的电子层结构与⑨元素的原子的电子层结构相同,这两种离子的半径由大到小的顺序是F->Na+(用相应离子符号作答).
(8)这些元素的最高价氧化物对应水化物呈两性的氢氧化物与氢氧化钠溶液反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ④ | ⑤ | ⑥ | ⑨ | ||||
| 3 | ① | ② | ③ | ⑦ | ⑧ |
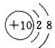 .
.(2)九种元素中非金属性最强的是F(填元素符号),元素⑧的氢化物的电子式为
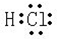 ,
,(3)除⑨外,原子半径最大的是Na(填元素符号).在①、②、③三种元素的最高价氧化物对应的水化物中,碱性最强的是NaOH(填化学式).电子式为
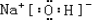 ,所含有的化学键类型有离子键、极性共价键,(请选择“离子键”、“极性共价键”、“非极性共价键”中的一个或几个填写).
,所含有的化学键类型有离子键、极性共价键,(请选择“离子键”、“极性共价键”、“非极性共价键”中的一个或几个填写).(4)⑥⑦⑧三种元素的气态氢化物的稳定性由强到弱的顺序是HF>HCl>H2S.(用相应的氢化物的化学式作答)
(5)元素④对应的氢化物的化学式是NH3,电子式为
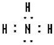 ,其水溶液的pH>7(填“<”或“>”).
,其水溶液的pH>7(填“<”或“>”).(6)⑦⑧两种元素对应的最高价含氧酸的酸性由强到弱的顺序是HClO4>H2SO4.(用相应的最高价氧化物对应水化物的化学式作答)
(7)①的阳离子与⑥的阴离子的电子层结构与⑨元素的原子的电子层结构相同,这两种离子的半径由大到小的顺序是F->Na+(用相应离子符号作答).
(8)这些元素的最高价氧化物对应水化物呈两性的氢氧化物与氢氧化钠溶液反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O.
7.下列说法不正确的是( )
| A. | 甲苯和环己烯都能使酸性高锰酸钾溶液褪色 | |
| B. | 用银氨溶液可以鉴别乙醛和葡萄糖溶液 | |
| C. | 甲醛和乙二醇都可作为合成高分子化合物的单体 | |
| D. | 丙烷和2-甲基丙烷的一氯代物均为两种 |
8.常温下,下列溶液中各微粒的物质的量浓度关系正确的是( )
| A. | 0.1 mol/L pH为4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-) | |
| B. | 相同条件下,pH=5的①NH4Cl溶液、②CH3COOH溶液、③稀盐酸三种溶液中由水电离出的c(H+):①>②>③ | |
| C. | 0.2mol/L的NaHCO3溶液与0.3 mol/L的Ba(OH)2溶液等体积混合,所得溶液中:c(OH-)>c(Ba2+)>c(Na+)>c(H+) | |
| D. | 等物质的量浓度的NaClO、NaHCO3混合溶液中:c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+c(CO32-) |
 将0.40mol N2O4气体充入2L固定容积的密闭容器中发生如下反应:N2O4(g)?2NO2(g)△H.在Tl℃和T2℃时,测得NO2的物质的量随时间变化如图所示:
将0.40mol N2O4气体充入2L固定容积的密闭容器中发生如下反应:N2O4(g)?2NO2(g)△H.在Tl℃和T2℃时,测得NO2的物质的量随时间变化如图所示: