题目内容
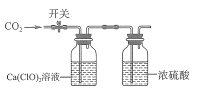
【题目】二氧化硫的污染臭名昭著,含硒的化学药物却有望迎来美名。某环保车间将含SO2、NO烟气经O3预处理后用CaSO3水悬浮液吸收。O3氧化烟气中SO2、NOx的主要反应的热化学方程式为
NO(g)+O3(g)=NO2(g)+O2(g) △H=-200.9 kJ·mol-1
NO(g)+1/2O2(g)=NO2(g) △H=-58.2 kJ·mol-1
SO2(g)+O3(g)=SO3(g)+O2(g) △H=-241.6kJ·mol-1
(1)实验表明,在常温下反应:3NO(g)+O3(g)=3NO2(g)正向自发,试说明原因:_____。
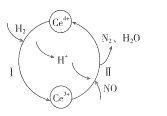
(2)将NO与H2的混合气体通入Ce(SO4)2与Ce2(SO4)3的混合溶液中,其转化过程如图所示,试写出反应I的离子反应方程式:___________,反应II的离子方程式:________________。
(3)用CaSO3水悬浮液处理二氧化氮,若在吸收液中加入Na2SO4溶液,能提高NO2的吸收速率,其主要原因是___________;达到平衡后,溶液中c(SO32-)=__________[用c(SO42-、Ksp(CaSO3)和Ksp(CaSO4)表示]。
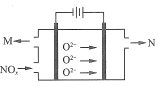
(4)氮的氧化物还可以通过电解法处理获得氮气和氧气,电解质为固体氧化物陶瓷,据图写出阴极的电极反应方程式:_______________。
(5)已知 SeO2与SO2的混合烟气用水吸收可制得单质硒,过滤得粗硒,硒的部分物理性质如下表所示。某工艺采用真空蒸馏的方法提纯获得纯硒,采用真空蒸馏的目的是_____。

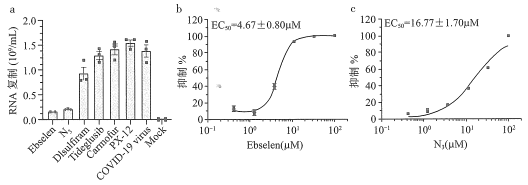
(6)最近我国学者锁定COVID-19的新靶点Mpro蛋白酶,通过先进筛选手段,在FDA批准的已上市和临床实验药物中,发现老药Ebselen(![]() )在细胞实验中展现出优异的抗病毒效果,优于此前研究者设计的多种冠状病毒Mpro蛋白酶的抑制剂N3,这两类药物都是抑制病毒的核苷酸的复制。Ebselen抑制病毒复制的最佳浓度为_____________
)在细胞实验中展现出优异的抗病毒效果,优于此前研究者设计的多种冠状病毒Mpro蛋白酶的抑制剂N3,这两类药物都是抑制病毒的核苷酸的复制。Ebselen抑制病毒复制的最佳浓度为_____________![]() ,比较N3半数有效浓度有无与伦比的优势。从影响化学反应速率的因素分析,这类药物的作用原理为_____________。
,比较N3半数有效浓度有无与伦比的优势。从影响化学反应速率的因素分析,这类药物的作用原理为_____________。
【答案】反应的△H=-317.3 kJ·mol-1,该反应是气体体积减小的反应,△S小于零,但数值很小,在常温下,△G=△H-T△S<0,反应自发 2Ce4++H2=2Ce3++2H+ 4H++2NO+4Ce3+=N2+4Ce4++2H2O CaSO3转化为CaSO4使溶液中SO32-的浓度增大,加快SO32-与NO2的反应速率 [Ksp(CaSO3)/Ksp(CaSO4)]×c(SO42-) 2NOx+4xe-=N2+2xO2- 降低Se的沸点,避免Se与空气中氧气发生反应 10 这类药物相当于病毒复制反应中的负催化剂,能明显的减缓反应速率,药物的有效特别强调催化剂的选择性,尽量不能影响人体健康
【解析】
(1)①NO(g)+O3(g)=NO2(g)+O2(g) △H=-200.9 kJ·mol-1,②NO(g)+1/2O2(g)=NO2(g) △H=-58.2 kJ·mol-1,利用盖斯定律,由反应①+2×②得3NO(g)+O3(g)=3NO2(g) △H=-317.3 kJ·mol-1,该反应是气体体积减小的反应,△S<0,但是数值很小,在常温下,△G=△H-T△S<0,反应自发;
(2)将NO与H2的混合气体通入Ce(SO4)2与Ce2(SO4)3的混合溶液中,根据转化过程的图示可知反应I是H2还原Ce4+,其离子方程式为2Ce4++H2=2Ce3++2H+;反应II的离子方程式:4H++2NO+4Ce3+=N2+4Ce4++2H2O ;
(3)加入Na2SO4溶液,发生反应CaSO3+SO42-=CaSO4+SO32-,CaSO3转化为CaSO4使溶液中SO32-的浓度增大,加速SO32-与NO2的反应速率, ,故溶液中c(SO32-)=[Ksp(CaSO3)/Ksp(CaSO4)]×c(SO42-);
,故溶液中c(SO32-)=[Ksp(CaSO3)/Ksp(CaSO4)]×c(SO42-);
(4)由题意可知NOx在阴极放电生成N2,电极反应式为2NOx+4xe-=N2+2xO2- ;
(5)真空使得压强降低,从而降低Se的沸点,避免Se与空气中氧气发生反应;
(6)由图b可知Ebselen浓度为10![]() 时出现拐点,且浓度再增大抑制率变化不大,故最佳浓度为10
时出现拐点,且浓度再增大抑制率变化不大,故最佳浓度为10![]() 。分析影响反应速率的因素,这类药物相当于病毒复制反应中的负催化剂,能明显的减缓反应速率,药物的有效特别强调催化剂的选择性,尽量不影响人体健康。
。分析影响反应速率的因素,这类药物相当于病毒复制反应中的负催化剂,能明显的减缓反应速率,药物的有效特别强调催化剂的选择性,尽量不影响人体健康。

【题目】HClO4、H2SO4、HNO3和HCl都是强酸,它们的酸性在水溶液中差别不大。以下是某温度下这四种酸在冰醋酸中的电离常数:
酸 | HClO4 | H2SO4 | HCl | HNO3 |
Ka | 1.6×10-5 | 6.3×10-9 | 1.6×10-9 | 4.2×10-10 |
下列说法中不正确的是( )
A.在冰醋酸中这四种酸都没有完全电离
B.在冰醋酸中HClO4是这四种酸中最强的酸
C.在冰醋酸中H2SO4的电离方程式为H2SO4===2H++SO![]()
D.水不能区分这四种酸的强弱,但冰醋酸可以区分这四种酸的强弱