��Ŀ����
����Ŀ��Fe(NO3)3��һ����Ҫ��ýȾ���ͽ������洦������������ˮ���Ҵ����������ᣬ���н�ǿ�������ԡ�ijѧϰС��������ͼװ���Ʊ�Fe(NO3)3��̽�������ʡ�
�ش��������⣺
����һ���Ʊ�Fe(NO3)3
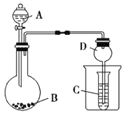
a�м���100mL8mol��L-1���ᣬb�м���5.6g��м������������м��Ϻ�ˮԡ���ȡ�
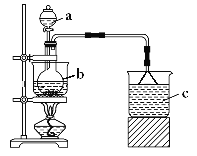
��1������b��������___��
��2����Ӧ�����й۲쵽b����м�ܽ⣬��Һ���ɫ��Һ���Ϸ��к���ɫ�������������b�з�Ӧ�����ӷ���ʽ��___��
��3��c����ʢ�Լ���___������©����������___��
��4����Ҫ�ӷ�Ӧ�����Һ�еõ�Fe(NO3)3���壬Ӧ��ȡ�IJ����ǣ�����Һ����Ũ������ȴ�ᾧ�����ˡ���____ϴ�ӡ����
�������̽��Fe(NO3)3������
i.���0.1mol��L-1Fe(NO3)3��Һ��pHԼ����1.6��
ii.��5mL0.1mol��L-1Fe(NO3)3��Һ�������������Թ��У�Լ1min��������ȫ�ܽ⡣
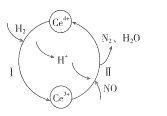
��5��ʹ�����ܽ��ԭ�������������a.NO3(H+)ʹ�����ܽ⣻b.__ʹ�����ܽ⡣Ϊ֤��b������������·�����ȡ���������ܽ�����Һ����һ֧�Թ��У�___��
���𰸡�Բ����ƿ Fe+3NO3-+6H+![]() Fe3++3NO2+3H2O NaOH��Һ ��ֹ���� �����HNO3 Fe3+ �μӼ������軯��[K3Fe(CN)6]��Һ��������ɫ�������ɣ����֤��ԭ��b����
Fe3++3NO2+3H2O NaOH��Һ ��ֹ���� �����HNO3 Fe3+ �μӼ������軯��[K3Fe(CN)6]��Һ��������ɫ�������ɣ����֤��ԭ��b����
��������
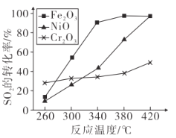
��1����ͼ֪����b�����ƣ�
��2���÷�Ӧ����������������������ˮ��
��3��c����ʢ�Լ������ն�������������©���������Ƿ�������
��4�������Ϣѡ��ϴ��Fe(NO3)3����ķ�����
��5��������֮�������������ʹ�����ܽ⣬��������Ӧ������T�ɣ�
��1������bΪԲ����ƿ��
��Ϊ��Բ����ƿ��
��2������ϡ���ᷴӦ����������������������ˮ�������ӷ���ʽΪ��Fe+3NO3-+6H+![]() Fe3++3NO2+3H2O��
Fe3++3NO2+3H2O��
����Fe+3NO3-+6H+![]() Fe3++3NO2+3H2O��
Fe3++3NO2+3H2O��
��3�����������ж�����һ�ֿ�����Ⱦ���c����ʢ�Լ���ѡNaOH��Һ���������ն������������屻���պ����������������©���������Ƿ�������
��Ϊ��NaOH��Һ����ֹ������
��4����Ŀ�ṩ��Ϣ��������������ˮ���Ҵ����������ᣬ��ѡ����ϴ��Fe(NO3)3�����ȥ�������������ʣ�
���������HNO3��
��5��������֮�⣬�����������Ҳ��ʹ�����ܽ⣬��Ŀ��ʾ���������н�ǿ�����ԣ����п��ܷ���Ag+Fe3+=Ag++Fe2+���ܽ�������ͨ��������Ӧ����������Ƿ�����������ӣ���ȡ��Ӧ�����Һ���μӼ������軯��[K3Fe(CN)6]��Һ��������ɫ�������ɣ����֤��ԭ��b������
��Ϊ��Fe3+���μӼ������軯��[K3Fe(CN)6]��Һ��������ɫ�������ɣ����֤��ԭ��b������

 ����ν����Ž̲��㽭���̴�ѧ������ϵ�д�
����ν����Ž̲��㽭���̴�ѧ������ϵ�д� �����Ļ������������������ϵ�д�
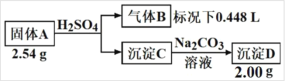
�����Ļ������������������ϵ�д�����Ŀ��.ij��ѧС��Ϊ���о���������Ի�ѧ��Ӧ���ʵ�Ӱ�죬����������ʵ�飺
��ʵ��ԭ����2KMnO4+5H2C2O4+3H2SO4=2MnSO4+10CO2��+K2SO4+8H2O
��ʵ�����ݼ���¼��
ʵ�� ��� | �����£��Թ��������Լ���������/mL | ��������Һ��ɫ������ɫ����ʱ��/min | |||
0.6mol/L H2C2O4 ��Һ | H2O | 0.2mol/LKMnO4��Һ | 3mol/Lϡ���� | ||
1 | 3.0 | 2.0 | 1.0 | 2.0 | 4.0 |
2 | 2.0 | 3.0 | 1.0 | 2.0 | 5.2 |
3 | 1.0 | 4.0 | 1.0 | 2.0 | 6.4 |
��ش�
��1�����ݱ��е�ʵ�����ݣ����Եõ��Ľ�����____��
��2������ʵ��1�����ݼ��㣬����ʱ������KMnO4��Ũ�ȱ仯��ʾ��ƽ����Ӧ����Ϊ��v(KMnO4)=____��
��3����С��ͬѧ���ݾ��������n(Mn2+)��ʱ��仯���Ƶ�ʾ��ͼ����ͼ1��ʾ������ͬѧ�������е�ʵ�����Ϸ��֣���ʵ�������n(Mn2+)��ʱ��仯������Ӧ��ͼ2��ʾ����С��ͬѧ����ͼ2��ʾ��Ϣ������µļ��裬����������ʵ��̽����
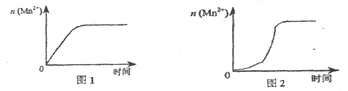
�ٸ�С��ͬѧ����ļ�����____��
�����������С��ͬѧ���ʵ�鷽��������д���пհס�
ʵ�� ��� | �����£��Թ��������Լ���������/mL | �����Թ��м����������� | ��������Һ��ɫ������ɫ����ʱ��/min | |||
0.6mol/LH2C2O4��Һ | H2O | 0.2mol/LKMnO4��Һ | 3mol/Lϡ���� | |||
4 | 3.0 | 2.0 | 1.0 | 2.0 | ___ | t |
������С��ͬѧ����ļ��������Ӧ�۲쵽��������______��