题目内容
【题目】恒温下,将amol N2与bmol H2的混合气体通入一个固定容积的密闭容器中,发生如下反应:N2(g)+3H2(g)![]() 2NH3(g), 已知反应进行到某时刻t时,nt(N2)=13mol,nt(NH3)=6mol; 反应达平衡时,混合气体的体积为716.8 L(标准状况下),其中NH3的体积分数为25%。则:
2NH3(g), 已知反应进行到某时刻t时,nt(N2)=13mol,nt(NH3)=6mol; 反应达平衡时,混合气体的体积为716.8 L(标准状况下),其中NH3的体积分数为25%。则:
(1)a的值为______。
(2)平衡时NH3的物质的量为___________。
(3)原混合气体与平衡混合气体的总物质的量之比(写出最简整数比,下同),n(始):n(平)=___________________。
(4)原混合气体中,a∶b=________。
(5)达到平衡时,N2和H2的转化率之比,α(N2)∶α(H2)=________。
(6)平衡混合气体中,n(N2)∶n(H2)∶n(NH3)=________。
【答案】 16 8mol 5∶4 2∶3 1∶2 3∶3∶2
【解析】(1)、根据方程式计算:
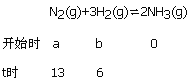
因t时生成6molNH3,则消耗了3molN2,所以a=13+3=16,故答案是:16。
(2)反应达平衡时,混合气体的物质的量为716.8L÷22.4L/mol=32mol,则NH3的物质的量为32mol×25%=8mol;故答案是:8mol。
(3)利用差量法计算:
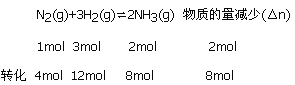
故原混合气体为32mol+8mol=40mol,则原混合气体与平衡混合气体的物质的量之比n(始):n(平)=40mol:32mol=5:4;故答案是5:4。
(4)由(1)知a=16mol,则b=40mol-16mol=24mol,所以a:b=16mol:24mol=2:3;故答案是2:3。
(5)达到平衡时,N2的转化率是α(N2)= ![]() ×100%=25%,H2的转化率α(H2)=
×100%=25%,H2的转化率α(H2)= ![]() ×100%=50%,所以达到平衡时,N2和H2的转化率之比:α(N2)∶α(H2)=25%:50%=1:2;故答案是1:2。
×100%=50%,所以达到平衡时,N2和H2的转化率之比:α(N2)∶α(H2)=25%:50%=1:2;故答案是1:2。
(6)平衡混合气的组成为:n(N2)=16mol-4mol=12mol,n(NH3)=8mol,n(H2)=32mol-12mol-8mol=12mol,平衡混合气体中,n(N2):n(H2):n(NH3)=12mol:12mol:8mol=3:3:2,故答案是3:3:2。