��Ŀ����
15�����������Ȼ�ѧ����ʽ�ó��Ľ�����ȷ���ǣ�������| A�� | ��֪2H2��g��+O2��g���T2H2O��l����H=-483.6 kJ•mol-1���� 2molH2��g����1molO2��g�������е���������2mol H2O��l�������е���������483.6kJ | |
| B�� | ��֪2C��s��+2O2��g���T2CO2��g����H12C��s��+O2��g��=2CO��g����H2�����H1����H2 | |
| C�� | ��֪C��ʯī��s��=C�����ʯ��s����H��0������ʯ��ʯī�ȶ� | |
| D�� | ���ø�˹���ɿ��Լ�Ӽ���ͨ��ʵ�����Բⶨ��Ӧ�ķ�Ӧ�� |
���� A����Ӧ�Ƿ��ȷ�Ӧ����Ӧ��������������������������
B��һ����̼ȼ�����ɶ�����̼���ȣ��ʱ�Ϊ��ֵ������
C����������Խ��Խ���ã�
D����˹����ʵ���ǻ�ѧ��Ӧ�ķ�Ӧ��ֻ�뷴Ӧ��ϵ��ʼ̬����̬�йأ����뷴Ӧ��;���أ�������Կ�������˹����ʵ�����ǡ����ܺ�����״̬��������һ���۵Ľ�һ�����֣�������һ���ɿ��Դ��Ѿ���ȷ�ⶨ�ķ�Ӧ��ЧӦ���������ڲ������ܲ����ķ�Ӧ����ЧӦ��
��� �⣺A����֪2H2��g��+O2��g���T2H2O��l����H=-483.6 kJ•mol-1����Ӧ�Ƿ��ȷ�Ӧ����Ӧ�������������������A����
B��һ����̼ȼ�����ɶ�����̼���ȣ��ʱ�Ϊ��ֵ����֪2C��s��+2O2��g���T2CO2��g����H12C��s��+O2��g��=2CO��g����H2�����H1����H2����B����
C����֪C��ʯī��s��=C�����ʯ��s����H��0����Ӧ�����ȷ�Ӧ�����ʯ��������ʯī����ʯī�Ƚ��ʯ�ȶ�����C����
D����˹����ʵ�����ǡ����ܺ�����״̬��������һ���۵Ľ�һ�����֣�������һ���ɿ��Դ��Ѿ���ȷ�ⶨ�ķ�Ӧ��ЧӦ���������ڲ������ܲ����ķ�Ӧ����ЧӦ����D��ȷ��
��ѡD��
���� ���⿼�����Ȼ�ѧ����ʽ����˹���ɵĺ����ʵ�ʣ����ջ����ǽ���ؼ�����Ŀ�ϼ�

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
��1���������Ũ���ᷴӦ�IJ���֮һ��TiOSO4����Ӧ�����������ɣ���д����Ӧ��ѧ����ʽ��FeTiO3+H2SO4��Ũ��=TiOSO4+FeSO4+2H2O��
��2����֪��TiO2+��ˮ�⣬ֻ�ܴ�����ǿ������Һ�У� 25��ʱ�����ܵ�����ܽ�ȣ�s����pH��ϵ��ͼ2��TiO��OH��2�ܶȻ�Ksp=1��10-29������Һ�в���c��TiO2+��=1.0��10-5 mol•L-1���������ҺpH����Ϊ3������������мԭ���ǽ�Fe3+ת��ΪFe2+����ֹFe3+��TiO2+ͬʱ���ɳ�����
��3������Һ����м��ȣ�ͬʱ����Na2CO3��ĩ�����ü��ȴٽ�TiO2++2H2O?TiO��OH��2+2H+ ���ƣ�Na2CO3��ĩ����H+���ٽ�TiO2+ˮ�⣻
��4���Ѱ�����������̿�ڸ����½��з�Ӧ��������һ�ֿ�ȼ����ɫ���壬д���÷�Ӧ�Ļ�ѧ����ʽ
TiO2+2Cl2+2C $\frac{\underline{\;����\;}}{\;}$ TiCl4+2CO�����������̹����У�����ѭ��ʹ�õ�����ΪH2SO4���ѧʽ��
��5��Mg��ԭTiCl4��Ӧ��õ�Mg��MgCl2��Ti�Ļ����ɲ����������ķ�������õ�Ti�������±���Ϣ������ȵ��¶��Ը���1412�漴�ɣ�
| TiCl4 | Mg | MgCl2 | Ti | |
| �۵�/�� | -25.0 | 648.8 | 714 | 1667 |
| �е�/�� | 136.4 | 1090 | 1412 | 3287 |
| A�� | 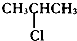 | B�� | CH3CH2Cl | C�� | 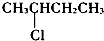 | D�� | CH3CH2CH2Cl |
| A�� | ���Ӱ뾶 Z��X | B�� | ���������� Z��Y | ||
| C�� | ������ Z��X | D�� | ԭ�Ӱ뾶 Z��Y |
����ϩ ������ ���ұ� �ܶ������� �ݾ���ϩ �ױ� �߱� �������ϩ��
| A�� | �ڢۢ� | B�� | �ڢۢݢޢߢ� | C�� | �ڢݢ� | D�� | �ڢ� |
| A�� | CuSO4+2NaOH�TCu��OH��2��+Na2SO4 | B�� | Cl2+H2O?HCl+HClO | ||
| C�� | Zn+H2SO4�TZnSO4+H2�� | D�� | 2Cu+O2$\frac{\underline{\;\;��\;\;}}{\;}$2CuO |
| A�� | �� | B�� | KCl��Һ | C�� | ������ | D�� | ����Cu��OH��2����Һ |
 ��·�ߣ�
��·�ߣ�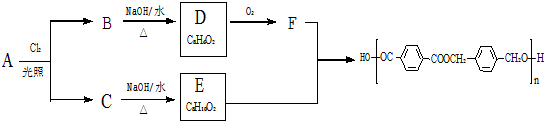
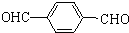 ����B����D�ķ�Ӧ���������ɵIJ��ȶ��м���Ľṹ��ʽ��
����B����D�ķ�Ӧ���������ɵIJ��ȶ��м���Ľṹ��ʽ��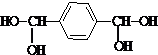 �����м�������D�ķ�Ӧ����Ϊ��ȥ��Ӧ��
�����м�������D�ķ�Ӧ����Ϊ��ȥ��Ӧ��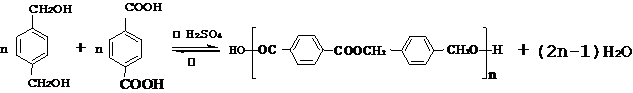 ����Ӧ����Ϊ���۷�Ӧ����E������ͬ�����ŵĺ�������ͬ���칹���У�д�ṹ��ʽ��
����Ӧ����Ϊ���۷�Ӧ����E������ͬ�����ŵĺ�������ͬ���칹���У�д�ṹ��ʽ��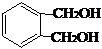 ��
��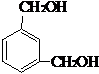 ��
��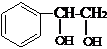 ��
��