题目内容
关于下列各装置图的叙述中,正确的是( )
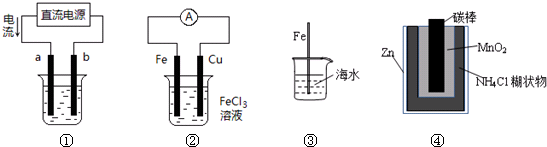

| A、用装置①精炼铜,则a极为粗铜,电解质溶液为CuSO4溶液 |
| B、装置②的总反应是:Cu+2Fe3+═Cu2++2Fe2+ |
| C、装置③中插入海水中的铁棒,越靠近底端腐蚀越严重 |
| D、装置④中Zn-MnO2干电池自放电腐蚀主要是由MnO2的氧化作用引起的 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:A.由电流方向可知a为阳极,精炼铜时,粗铜为阳极,纯铜为阴极;
B.铁为负极,与Fe3+发生氧化还原反应;
C.金属发生腐蚀,应有氧气参加反应;
D.锌被氧化,正极发生还原反应,生成氢气.
B.铁为负极,与Fe3+发生氧化还原反应;
C.金属发生腐蚀,应有氧气参加反应;
D.锌被氧化,正极发生还原反应,生成氢气.
解答:
解:A.由电流方向可知a为阳极,精炼铜时,粗铜为阳极,纯铜为阴极,符合精炼的装置特点,故A正确;
B.铁为负极,与Fe3+发生氧化还原反应,总反应式为Fe+2Fe3+═3Fe2+,故B错误;
C.越靠近底端,氧气越少,越不易腐蚀,故C错误;
D.锌被氧化,正极发生还原反应,由于氯化铵水解呈酸性,正极上氢离子得到电子被还原生成氢气,故D错误.
故选A.
B.铁为负极,与Fe3+发生氧化还原反应,总反应式为Fe+2Fe3+═3Fe2+,故B错误;
C.越靠近底端,氧气越少,越不易腐蚀,故C错误;
D.锌被氧化,正极发生还原反应,由于氯化铵水解呈酸性,正极上氢离子得到电子被还原生成氢气,故D错误.
故选A.
点评:本题综合考查原电池、电解池知识,为高考常见题型和高频考点,侧重于学生的分析能力的考查,注意把握电解池与原电池的工作原理以及电极方程式的书写,难度不大,注意相关基础知识的积累.

练习册系列答案
 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案
相关题目
下列各组中的离子因发生氧化还原反应而不能大量共存的是( )
| A、H+、Na+、CO32-、Cl- |
| B、Ca2+、K+、S2-、ClO- |
| C、Fe2+、CO32-、Cl-、NO3- |
| D、HCO3-、Br-、OH-、SO42- |
下列反应属于氧化还原反应的是( )
| A、Ba(OH)2+H2SO4=BaSO4↓+2H2O | ||||
B、Fe2O3+3CO
| ||||
| C、2NaHCO3=Na2CO3+CO2↑+H2O | ||||
| D、Na2O+H2O=2NaOH |
900℃时,向2.0L恒容密闭容器中充入0.40mol乙苯,发生反应为:
 ?
? (g)+H2(g)△H=a kJ?mol-1.
(g)+H2(g)△H=a kJ?mol-1.
经一段时间后达到平衡.反应过程中测定的部分数据见下表:
下列说法正确的是( )
 ?
? (g)+H2(g)△H=a kJ?mol-1.
(g)+H2(g)△H=a kJ?mol-1.经一段时间后达到平衡.反应过程中测定的部分数据见下表:
| 时间/min | 0 | 10 | 20 | 30 | 40 |
| n(乙苯)/mol | 0.40 | 0.30 | 0.24 | n2 | n3 |
| n(苯乙烯)/mol | 0.00 | 0.10 | n1 | 0.20 | 0.20 |
| A、反应在前20min的平均速率为v(H2)=0.008mol?L-1?min-1 |
| B、保持其他条件不变,升高温度,平衡时,c(乙苯)=0.08mol?L-1,则a<0 |
| C、保持其他条件不变,再向容器中充入0.40mol乙苯和0.40mol H2,平衡不移动 |
| D、达平衡状态的标志是气体密度不再变化 |
下列灭火剂能用于扑灭金属钠着火的是( )
| A、干冰灭火剂 |
| B、黄砂 |
| C、干粉(含NaHCO3)灭火剂 |
| D、泡沫灭火剂 |
常温下,下列有关溶液中微粒的物质的量浓度关系正确的是( )
| A、0.1mol/L (NH4)2Fe(SO4)2溶液中:c(NH4+)+c(NH3?H2O)+c(Fe2+)=0.3mol/L |
| B、0.1mol?L-1 NH4HS溶液中:c(NH4+)<c(HS-)+c(H2S)+c(S2-) |
| C、pH=8.0的KHS溶液中:c(K+)>c(HS-)>c(OH)>c(S2)>c(H+) |
| D、常温下,将10mL 0.1mol?L-1的盐酸与20mL 0.1mol?L-1的氨水混合,所得溶液中:c(NH3?H2O)>c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
在下列物质中,硫元素为+4价的是( )
| A、H2S |
| B、SO2 |
| C、S |
| D、H2SO4 |
低温脱硝技术可用于处理废气中的氮氧化物,发生的化学反应为:2NH3(g)+NO(g)+NO2(g)
2N2(g)+3H2O(g)△H<0在恒容的密闭容器中,下列有关说法不正确的是( )
| 180℃ |
| 催化剂 |
| A、每转化掉1mol NO和1mol NO2混合气体,反应转移6mol电子 |
| B、升高温度,可使该反应的反应速率增大 |
| C、平衡时,其他条件不变,升高温度则该反应的平衡常数减少 |
| D、其他条件不变,使用高效催化剂平衡会发生移动,氮氧化物的转化率增大 |