题目内容
在下列物质中,硫元素为+4价的是( )
| A、H2S |
| B、SO2 |
| C、S |
| D、H2SO4 |
考点:根据化学式判断化合价
专题:氧化还原反应专题
分析:根据化合物中正负化合价代数和为零,结合各选项中的化学式进行解答本题
解答:
解:A.氢元素显+1价,设H2S中硫元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)×2+x=0,则y=-2价,故A错误;
B.氧元素显-2价,设SO2中硫元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:x+(-2)×2=0,则x=+4价,故B正确;
C.单质硫的化合价是0价,故C错误;
D.氢元素显+1价,氧元素显-2价,设H2SO4中硫元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)×2+x+(-2)×4=0,则y=+6价,故D错误,
故选B.
B.氧元素显-2价,设SO2中硫元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:x+(-2)×2=0,则x=+4价,故B正确;
C.单质硫的化合价是0价,故C错误;
D.氢元素显+1价,氧元素显-2价,设H2SO4中硫元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)×2+x+(-2)×4=0,则y=+6价,故D错误,
故选B.
点评:本题考查化合物中元素化合价的有关计算,难度不大,关键要把握化合物中正负化合价代数和为零这一规律.

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
下列说法中正确的是( )
| A、除去乙烷中混有的乙烯的方法是通氢气在一定条件下反应,使乙烯转化为乙烷 |
| B、苯、溴苯在常温、常压下为无色且密度比水小的液体 |
| C、丙烯与2-丁烯都存在順反异构体 |
| D、苯不能与溴水发生加成反应,也不能被酸性KMnO4溶液氧化 |
下列说法不正确的是( )
| A、胶体能发生电泳现象是因为胶体带电 |
| B、生石灰与水混合的过程只发生物理变化 |
| C、O3是由3个氧原子构成的化合物 |
| D、CuSO4?5H2O是一种混合物 |
关于下列各装置图的叙述中,正确的是( )
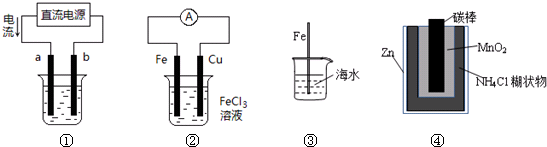

| A、用装置①精炼铜,则a极为粗铜,电解质溶液为CuSO4溶液 |
| B、装置②的总反应是:Cu+2Fe3+═Cu2++2Fe2+ |
| C、装置③中插入海水中的铁棒,越靠近底端腐蚀越严重 |
| D、装置④中Zn-MnO2干电池自放电腐蚀主要是由MnO2的氧化作用引起的 |
下列各种冶炼方法中,可制得相应的金属的是( )
| A、电解熔融氯化铝制铝 |
| B、加热氧化银制银 |
| C、电解氯化钠溶液制钠 |
| D、氯化钠与铝粉高温共热制钠 |
有温度、容积相同的甲、乙两个密闭容器.往甲容器中通入1g N2和1g H2,乙容器中通入2g N2和2g H2,保持恒温、恒容达到平衡,相关参数比较正确的是( )
| A、平衡时N2的转化率:α甲>2α乙 |
| B、平衡时NH3的浓度:2c甲<c乙 |
| C、平衡时体系压强:2p甲>p乙 |
| D、反应放出的热量:2Q甲>Q |
下列选项的说法中正确的是( )
| A、分子的结构是由键角决定的 |
| B、共价键的键能越大,共价键越牢固 |
| C、CF4、CCl4、CBr4、CI4中C-X键的键长、键角均相等 |
| D、H2O分子中的两个O-H键的键角为180° |
下列说法正确的是( )
| A、14C的中子数为14 |
| B、14C的质子数为14 |
| C、14C和12C互为同位素 |
| D、14CO2的摩尔质量为46 |
100mL Al2(SO4)3、K2SO4、KAl(SO4)2的混合液中,如果SO42-的浓度等于0.4mol/L,当加入2mol/L的KOH溶液50mL时,生成沉淀恰好溶解,则原混合物中K+的物质的量浓度是( )
| A、0.2mol?L-1 |
| B、0.05mol?L-1 |
| C、0.45mol?L-1 |
| D、0.225mol?L-1 |