题目内容
下列各组中的离子因发生氧化还原反应而不能大量共存的是( )
| A、H+、Na+、CO32-、Cl- |
| B、Ca2+、K+、S2-、ClO- |
| C、Fe2+、CO32-、Cl-、NO3- |
| D、HCO3-、Br-、OH-、SO42- |
考点:离子共存问题
专题:离子反应专题
分析:具有还原性的离子与具有氧化性的离子发生氧化还原反应,则不能共存,以此来解答.
解答:
解:A.H+、CO32-结合生成水和气体,因复分解反应不能共存,故A不选;
B.S2-、ClO-发生氧化还原反应,不能共存,故B选;
C.Fe2+、CO32-相互促进水解生成沉淀和气体,不能共存,故C不选;
D.HCO3-、OH-结合生成水和碳酸根离子,因复分解反应不能共存,故D不选;
故选B.
B.S2-、ClO-发生氧化还原反应,不能共存,故B选;
C.Fe2+、CO32-相互促进水解生成沉淀和气体,不能共存,故C不选;
D.HCO3-、OH-结合生成水和碳酸根离子,因复分解反应不能共存,故D不选;
故选B.
点评:本题考查离子的共存,为高频考点,把握常见离子的性质及不能共存的原因为解答的关键,涉及水解、复分解、氧化还原反应的考查,题目难度不大.

练习册系列答案
相关题目
下列说法正确的是( )
| A、在100℃、101kPa条件下,1mol液态水气化时需要吸收40.69kJ的热量,则H2O(g)?H2O(l)的△H=+40.69kJ?mol-1 | ||||||||
| B、已知CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=-802.33kJ/mol,则CH4的燃烧热为802.33kJ | ||||||||
C、H2(g)+Br2(g)═2HBr(g)△H=-72kJ?mol-1其它相关数据如表:
| ||||||||
| D、已知S(g)+O2(g)=SO2(s);△H1,S(g)+O2(g)=SO2(g);△H2,则△H2<△H1 |
欲除去CuSO4?5H2O中的沙子(主要成分为SiO2),必要的实验操作为( )
| A、溶解 过滤 蒸发结晶 |
| B、加热 溶解 过滤 |
| C、溶解 过滤 蒸馏 |
| D、溶解 过滤 分液 |
关于下列各图的叙述正确的是( )
A、 表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为483.6kJ?mol-1 |
B、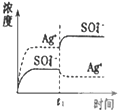 表示向Ag2SO4饱和溶液中加入等体积Na2SO4稀溶液,平衡会向左移动,Ksp减小 |
C、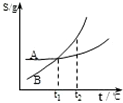 表示A、B两物质的溶解度随温度变化情况,将A、B饱和溶液分别由t1℃升温至t2℃时,溶质的质量分数B>A |
D、 表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则同浓度的NaA溶液的pH小于NaB溶液 |
根据物质的组成对物质进行分类,Na2CO3属于( )
| A、盐 | B、有机物 | C、碱 | D、氧化物 |
下列说法中正确的是( )
| A、除去乙烷中混有的乙烯的方法是通氢气在一定条件下反应,使乙烯转化为乙烷 |
| B、苯、溴苯在常温、常压下为无色且密度比水小的液体 |
| C、丙烯与2-丁烯都存在順反异构体 |
| D、苯不能与溴水发生加成反应,也不能被酸性KMnO4溶液氧化 |
在离子浓度都为0.1mol/L的下列溶液中,加入(或通入)某物质后,发生反应先后顺序正确的是( )
| A、在含Fe3+、Cu2+、H+的溶液中加入锌粉:Cu2+、Fe3+、H+ |
| B、在含I-、SO32-、Br-的溶液中不断通入氯气:I-、Br-、SO32- |
| C、在含AlO2-、SO32-、OH-的溶液中逐滴加入硫酸氢钠溶液:OH-、AlO2-、SO32- |
| D、在含Fe3+、H+、NH4+的溶液中逐渐加入烧碱溶液:H+、NH4+、Fe3+ |
关于下列各装置图的叙述中,正确的是( )
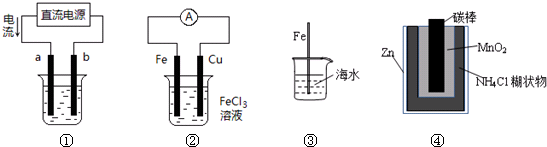

| A、用装置①精炼铜,则a极为粗铜,电解质溶液为CuSO4溶液 |
| B、装置②的总反应是:Cu+2Fe3+═Cu2++2Fe2+ |
| C、装置③中插入海水中的铁棒,越靠近底端腐蚀越严重 |
| D、装置④中Zn-MnO2干电池自放电腐蚀主要是由MnO2的氧化作用引起的 |