题目内容
【题目】强酸制弱酸非常重要的一种离子反应,已知:
Ka1 | Ka2 | |
H2SO3 |
|
|
H2CO3 |
|
|
下列离子反应不正确的有( )个
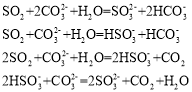
A.0个B.1个C.2个D.3个
【答案】B
【解析】
根据K大小得出酸强弱顺序为H2SO3 > H2CO3> HSO3- > HCO3-。由于H2SO3 >H2CO3> HSO3-,因此SO2 + CO32 + H2O = HSO3- + HCO3-,由于H2CO3 >HSO3- > HCO3-,因此HSO3- + CO32 = SO32 + HCO3-,两个方程式相加得到SO2 +2CO32 + H2O = SO32 + 2HCO3-,故第一个、第二个正确;由于H2CO3> HSO3-,因此SO2 + CO32 + H2O = HSO3- + HCO3-,由于H2SO3 > H2CO3,因此SO2 + HCO3- = HSO3- + CO2,两个方程式相加2SO2 + CO32 + H2O = 2HSO3- + CO2,故第三个正确;2HSO3- + CO32 = CO2+ H2O + 2SO32违背了H2CO3> HSO3-,故第四个错误,故B正确。
综上所述,答案为B。

【题目】温度为T时,向2.0L恒容密闭容器中充入1.0mol PCl5,反应PCl5(g)PCl3(g)+Cl2(g),经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
下列说法正确的是( )
A.反应在50s时的速率v(PCl3)=0.0016molL﹣1s﹣1
B.保持其他条件不变,升高温度,平衡时c(PCl3)=0.11molL﹣1,则反应的△H<0
C.相同温度下,起始时向容器中充入1.0molPCl5、0.20molPCl3和0.20molCl2,反应达到平衡前v(正)>v(逆)
D.相同温度下,起始时向容器中充入2.0molPCl3和2.0molCl2,达到平衡时,PCl3的转化率小于80%