题目内容
【题目】铁氮化合物(FexNy)在磁记录材料领域有着广泛的应用前景。请回答下列问题:
(1)铁元素基态原子的电子排布式为_________,3d能级上的未成对电子数为_________,能量最高能级的电子云形状为_________。
(2)Fe3+可用KSCN溶液检验,形成的配合物颜色为_________,写出一个与SCN-具有相同空间构型的分子:_________。
(3)氮元素的最简单氢化物为氨,氨的沸点_________(填“高于”或“低于”)膦(PH3),原因是_________。氮元素另一种氢化物联氨(N2H4)是_________(填“极性”或“非极性”)分子,其中心原子的轨道杂化类型为_________。
(4)铁的第三电离能(I3),第四电离能(I4)分别为2957kJ/mol,5290kJ/mol,I4远大于I3的原因是_________。
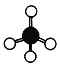
(5)铁和氨气在640℃可发生置换反应,产物之一的晶胞结构如图所示,写出该反应的化学方程式:_________。若两个最近的Fe原子间的距离为a cm,则该晶体的密度是_________g/cm3(设阿伏加德罗常数的值为NA)。

【答案】[Ar]3d64s2 4 花瓣形 红色 CO2或CS2 高于 NH3分子间存在氢键,导致沸点高于PH3 极性 sp3 Fe3+的3d能级半充满,结构稳定 8Fe+3NH3![]() 2Fe4N+3H2
2Fe4N+3H2 ![]()
【解析】
(1)铁元素为26号元素,位于第四周期第Ⅷ族,其基态原子的电子排布式为1s22s22p63s23p63d64s2或[Ar]3d64s2;d能级有5个原子轨道,按照洪特规则和泡利原理,因此铁元素的3d能级上未成对电子数为4;按照构造原理,能量最高能级为3d,其电子云形状为花瓣形;
(2)Fe3+与SCN-形成配合物,其配合物的颜色为(血)红色;利用等电子体具有相似化学结构和化学键特征,SCN-与CO2互为等电子体,即SCN-的空间构型为直线型,与之相似的还有CS2等;
(3)氨分子间能形成分子间氢键,其沸点高于不含分子间氢键的PH3;N2H4的结构式为 ,肼分子含有极性键和非极性键,每个氮原子都与相邻的原子形成变形的三角锥形,氮氮单键可以旋转,不一定是对称结构,因此肼为极性分子;N有三个σ键,一个孤电子对,因此杂化类型为sp3;
,肼分子含有极性键和非极性键,每个氮原子都与相邻的原子形成变形的三角锥形,氮氮单键可以旋转,不一定是对称结构,因此肼为极性分子;N有三个σ键,一个孤电子对,因此杂化类型为sp3;
(4)Fe失去3个电子后,Fe3+电子排布式为[Ar]3d5,d能级处于半满,能量低,处于稳定;
(5)根据晶胞的结构,Fe位于顶点和面心,个数为8×1/8+6×1/2=4,N位于晶胞内部,该晶胞的化学式为Fe4N,铁和NH3在640℃可发生置换反应,反应方程式为8Fe+3NH3![]() 2Fe4N+3H2,根据晶胞的结构,两个最近的Fe原子间的距离是面对角线的一半,即晶胞的边长为
2Fe4N+3H2,根据晶胞的结构,两个最近的Fe原子间的距离是面对角线的一半,即晶胞的边长为![]() acm,晶胞的质量为1×(56×4+14)/NAg,根据密度定义,得出该晶胞的密度为
acm,晶胞的质量为1×(56×4+14)/NAg,根据密度定义,得出该晶胞的密度为![]() g/cm3。
g/cm3。

 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案【题目】以方潜矿(PbS)为原料制备铅蓄电池的电极材料的工艺流程如图所示:

部分化合物的Ksp如下表所示:
物质 | PbCl2 | PbS | PbCrO4 |
Ksp | 1.2×10-5 | 9.0×10-29 | 1.8×10-14 |
请回答下列问题:
(1)“焙烧”生成的气体可用于工业制备____________。
(2)写出“高温还原”的主要化学方程式:____________。
(3)“粗铅”的杂质主要有锌,铁,铜,银等,电解精炼时阴极反应式为____________。阳极泥的主要成分为____________。
(4)铅与稀盐酸反应产生少量气泡后反应终止,原因是____________。写出制备PbO2的离子方程式:____________。
(5)Pb(NO3)2是强酸弱碱盐,氢硫酸(H2S)是弱酸,向Pb(NO3)2溶液中通入H2S气体是否能产生黑色PbS沉淀____________?(列式计算说明,Ka1(H2S)=1.3×10-7,Ka2(H2S)=7.1×10-15)。
(6)将PbCrO4加入足量硝酸中,部分振荡,观察到主要现象是____________,反应的离子方程式为____________。