题目内容
下列推断正确的是( )
| A、SiO2能与NaOH溶液、HF溶液反应,所以SiO2是两性氧化物 |
| B、新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色 |
| C、CO、NO、NO2都是大气污染气体,在空气中都能稳定存在 |
| D、Na2O、Na2O2组成元素相同,阳离子与阴离子个数比也相同 |
考点:硅和二氧化硅,氯气的化学性质,氮的氧化物的性质及其对环境的影响,钠的重要化合物
专题:元素及其化合物
分析:A.根据两性氧化物的定义判断;
B.氯水中含有次氯酸,具有漂白性;
C.NO在空气中不能稳定存在;
D.Na2O、Na2O2的阴离子分别为O2-、O22-.
B.氯水中含有次氯酸,具有漂白性;
C.NO在空气中不能稳定存在;
D.Na2O、Na2O2的阴离子分别为O2-、O22-.
解答:
解:A.两性氧化物与酸或碱反应都能生成盐和水,而二氧化硅与氢氟酸反应生成四氟化硅与水,没有生成盐,所以不是两性氧化物,故A错误;
B.氯水中含有次氯酸,具有漂白性,可使紫色石蕊试液先变红,后褪色,故B错误;
C.NO在空气中不能稳定存在,易与氧气反应生成二氧化氮,故C错误;
D.Na2O、Na2O2的阴离子分别为O2-、O22-,阳离子与阴离子个数比相同,故D正确.
故选D.
B.氯水中含有次氯酸,具有漂白性,可使紫色石蕊试液先变红,后褪色,故B错误;
C.NO在空气中不能稳定存在,易与氧气反应生成二氧化氮,故C错误;
D.Na2O、Na2O2的阴离子分别为O2-、O22-,阳离子与阴离子个数比相同,故D正确.
故选D.
点评:本题考查较为综合,涉及二氧化硅、氯水、NO以及过氧化钠等知识,为高考常见题型,侧重于学生的分析能力和元素化合物知识的综合理解和运用的考查,难度不大,注意相关基础知识的积累.

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案
相关题目
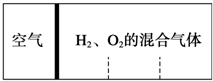 如图所示,分别向密闭容器内可移动活塞的两边充入空气(已知空气体积占整个容器容积的
如图所示,分别向密闭容器内可移动活塞的两边充入空气(已知空气体积占整个容器容积的| 1 |
| 4 |
| A、2:7 | B、5:4 |
| C、2:1 | D、4:5 |
下列叙述正确的是( )
| A、元素处于最高价态时一定有强氧化性;同理元素处于最低价态时一定具有强还原性 |
| B、将FeCl2溶液与稀HNO3混合离子反应方程式:Fe2++4H++NO3-═Fe3++NO↑+2H2O |
| C、HF、Al(OH)3、氨水都是弱电解质 |
| D、颜色反应、显色反应、指示剂变色反应均属化学变化 |
设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A、7.8g Na2O2含有的阴离子数目为0.2NA |
| B、电解精炼铜时每转移NA个电子,阳极溶解32g铜 |
| C、14g乙烯和丙烯(C3H6)的混合物中含有的原子数目为3NA |
| D、1L 0.5mol/L Na2CO3溶液中含有的CO32-数目为0.5NA |
下列各表述与示意图一致的是( )
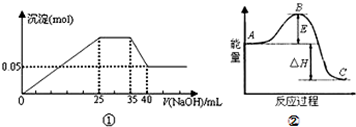

| A、图①表示向含Mg2+、Al3+、NH4+的盐溶液中滴加NaOH溶液时,沉淀的量与NaOH的体积的关系图.则三种离子的物质的量之比为:n(Mg2+):n(Al3+):n( NH4+)=2:1:2 |
| B、图①中使用的NaOH的浓度为2mol?L-1 |
| C、图②中物质A反应生成物质C,△H>0 |
| D、图②中曲线表示某反应过程的能量变化,若使用催化剂,E值会减小 |
下列实验操作中正确的是( )
| A、蒸发操作时,应将蒸发皿放在石棉网上进行加热 |
| B、焰色反应实验中可用铜丝代替铂丝完成实验 |
| C、分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
| D、向1mol?L-1氯化铁溶液中加入少量的NaOH溶液制取氢氧化铁胶体 |
下列叙述中全部为不正确的组合是( )
(1)纯铁比碳素钢易生锈
(2)用氨水除去试管上的银镜
(3)硅是制作光导纤维和制造太阳能电池的主要原料
(4)可用稀盐酸、碳酸钠溶液、硅酸钠溶液设计实验来验证元素的非金属性Cl>C(碳)>Si
(5)催化剂只能改变反应的活化能,不能改变反应的热效应
(6)用氢氟酸雕刻玻璃是利用氢氟酸能与二氧化硅反应的性质
(7)同主族元素的简单阴离子还原性越强,水解程度越大
(8)Al2O3在工业上用于制作耐高温材料,也用于电解法治炼铝
(9)丁达尔效应可用于区别溶液与胶体,云、雾均能产生丁达尔效应
(10)明矾可用于水的消毒、杀菌;碳酸钡可用于钡餐透视
(11)用浸泡过的高锰酸钾溶液的硅藻土吸收水果释放的乙烯,可达到水果保鲜的目的
(12)同周期金属元素的化合价越高,其原子失电子能力越弱.
(1)纯铁比碳素钢易生锈
(2)用氨水除去试管上的银镜
(3)硅是制作光导纤维和制造太阳能电池的主要原料
(4)可用稀盐酸、碳酸钠溶液、硅酸钠溶液设计实验来验证元素的非金属性Cl>C(碳)>Si
(5)催化剂只能改变反应的活化能,不能改变反应的热效应
(6)用氢氟酸雕刻玻璃是利用氢氟酸能与二氧化硅反应的性质
(7)同主族元素的简单阴离子还原性越强,水解程度越大
(8)Al2O3在工业上用于制作耐高温材料,也用于电解法治炼铝
(9)丁达尔效应可用于区别溶液与胶体,云、雾均能产生丁达尔效应
(10)明矾可用于水的消毒、杀菌;碳酸钡可用于钡餐透视
(11)用浸泡过的高锰酸钾溶液的硅藻土吸收水果释放的乙烯,可达到水果保鲜的目的
(12)同周期金属元素的化合价越高,其原子失电子能力越弱.
| A、(1)(4)(5)(6)(7)(11) |
| B、(2)(3)(5)(7)(9)(12) |
| C、(1)(2)(3)(4)(7)(10) |
| D、(2)(6)(8)(10)(11)(12) |
下列说法正确的是( )
A、化合物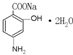 的核磁共振氢谱测出5个谱峰 的核磁共振氢谱测出5个谱峰 |
| B、实验室检验NH4HCO3溶液中NH4+的方法是取少量溶液,加热,并用湿润的红色石蕊试纸检证产生的气体,试纸变蓝,证明有NH4+ |
| C、在一定条件下,某可逆反应的△H=+100kJ?mol-1,则该反应正反应活化能比逆反应活化能大100kJ?mol-1 |
| D、等浓度的碳酸钠和碳酸氢钠溶液混合后的溶液中:2c(OH-)+c(CO32-)=c(HCO3-)+3c(H2CO3)+2c(H+) |