题目内容
设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A、7.8g Na2O2含有的阴离子数目为0.2NA |
| B、电解精炼铜时每转移NA个电子,阳极溶解32g铜 |
| C、14g乙烯和丙烯(C3H6)的混合物中含有的原子数目为3NA |
| D、1L 0.5mol/L Na2CO3溶液中含有的CO32-数目为0.5NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、依据n=
计算物质的量,结合过氧化钠是钠离子和过氧根离子构成计算分析;
B、电解精炼铜时,粗铜做阳极,精铜做阴极,阳极上铜、锌、铁等金属失电子,阴极析出铜,结合电子守恒分析;
C、乙烯和丙烯最简式为CH2,计算14gCH2中含有原子数;
D、碳酸根离子水解;
| m |
| M |
B、电解精炼铜时,粗铜做阳极,精铜做阴极,阳极上铜、锌、铁等金属失电子,阴极析出铜,结合电子守恒分析;
C、乙烯和丙烯最简式为CH2,计算14gCH2中含有原子数;
D、碳酸根离子水解;
解答:
解:A、7.8g Na2O2物质的量=
=0.1mol,过氧化钠是钠离子和过氧根离子构成,含有的阴离子数目为0.1NA ,故A错误;
B、电解精炼铜时,粗铜做阳极,精铜做阴极,阳极上铜、锌、铁等金属失电子,阴极析出铜,每转移NA个电子,阳极溶解铜质量小于32g,故B错误;
C、乙烯和丙烯最简式为CH2,计算14gCH2中含有原子数=
=1mol,含有的原子数目为3NA,故C正确;
D、1L 0.5mol/L Na2CO3溶液中,溶质物质的量=1L×0.5mol/L=0.5mol,碳酸根离子水解,含有的CO32-数目小于0.5NA,故D错误;
故选C.
| 7.8g |
| 78g/mol |
B、电解精炼铜时,粗铜做阳极,精铜做阴极,阳极上铜、锌、铁等金属失电子,阴极析出铜,每转移NA个电子,阳极溶解铜质量小于32g,故B错误;
C、乙烯和丙烯最简式为CH2,计算14gCH2中含有原子数=
| 14g |
| 14g/mol |
D、1L 0.5mol/L Na2CO3溶液中,溶质物质的量=1L×0.5mol/L=0.5mol,碳酸根离子水解,含有的CO32-数目小于0.5NA,故D错误;
故选C.
点评:本题考查了阿伏伽德罗常数的分析应用,主要是电解精炼的计算分析,物质结构、盐类水解特征判断,掌握基础是关键,题目较简单.

练习册系列答案
 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案
相关题目
用NA表示阿伏加德罗常数的值.下列叙述中不正确的是( )
| A、分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA |
| B、1L 1mol?L-1FeCl3溶液中Fe3+的数目小于NA |
| C、在18g 18O2中含有NA个氧原子 |
| D、22.4L氯气与足量镁粉充分反应,转移的电子数为2NA |
不能由单质直接化合得到的物质是( )
| A、Cu2S |
| B、FeCl2 |
| C、FeS |
| D、Al2S3 |
下列物质中能与NaOH溶液反应的是( )
| A、Mg | B、Fe | C、Al | D、Cu |
有3份等质量的小苏打,第1份直接与过量过酸反应;第2份先加热,使其部分分解后,再与过量盐酸反应;第3份先加热,使其完全分解后,再与过量盐酸反应.假若盐酸的物质的量浓度相同,实际消耗盐酸的体积分别为V1、V2和V3,则V1、V2和V3的大小关系正确的是( )
| A、V2>V3>V1 |
| B、V1>V3>V2 |
| C、V1=V2=V3 |
| D、V1>V2>V3 |
下列推断正确的是( )
| A、SiO2能与NaOH溶液、HF溶液反应,所以SiO2是两性氧化物 |
| B、新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色 |
| C、CO、NO、NO2都是大气污染气体,在空气中都能稳定存在 |
| D、Na2O、Na2O2组成元素相同,阳离子与阴离子个数比也相同 |
下列措施或事实不能用勒夏特列原理解释的是( )
| A、在合成氨的反应中,降温或加压有利于氨的合成 |
| B、H2、I2、HI平衡混合气加压后颜色变深 |
| C、Fe(SCN)3溶液中加入固体KSCN后颜色变深 |
| D、阴暗处密封有利于氯水的储存 |
化学中常用图象直观地描述化学反应的进程或结果,下列图象描述正确的是( )
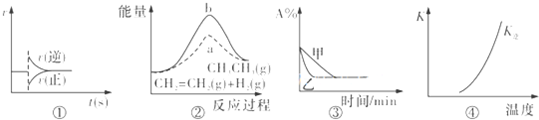

| A、图①可以表示某化学平衡体系改变温度后,反应速率随时间的变化 |
| B、图②中a、b曲线分别表示反应CH2═CH2(g)+H2(g)→CH3CH3(g)△H<0未使用和使用催化剂时,反应过程中的能量变化 |
| C、图③表示压强对可逆反应2A(g)+2B(g)?3C(g)+D(g)影响,且甲的压强大 |
| D、图④中曲线表示反应2SO2(g)+O2(g)?2SO3(g)△H<0反应的平衡常数K随温度的变化 |
下列氧化还原反应中,电子得失情况表示不正确的是( )
A、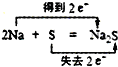 |
B、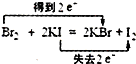 |
C、 |
D、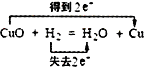 |