题目内容
【题目】在![]() 时,将
时,将![]() 、
、![]() 分别充入两个各为
分别充入两个各为![]() 的密闭容器中,反应过程中浓度变化如下:
的密闭容器中,反应过程中浓度变化如下:![]() ,下列说法正确的是
,下列说法正确的是![]()
容器 | 物质 | 起始浓度 | 平衡浓度 |
Ⅰ |
|
|
|
| 0 |
| |
Ⅱ |
| 0 |
|
|
|
|
A.平衡时,Ⅰ、Ⅱ中反应物的转化率![]()
B.平衡时,Ⅰ、Ⅱ中上述正反应的平衡常数![]() Ⅰ
Ⅰ![]() Ⅱ
Ⅱ![]()
C.平衡后,Ⅰ中加入![]() 的
的![]() ,达到新平衡时,反应物的转化率
,达到新平衡时,反应物的转化率![]() 增大
增大
D.平衡后,升高温度,Ⅰ、Ⅱ中气体颜色都将变深
【答案】D
【解析】
由表中数据可知,容器I中

容器II中,
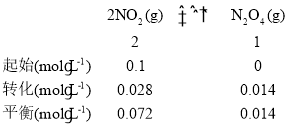
A、平衡时,Ⅰ中反应物的转化率![]() ,Ⅱ中反应物的转化率
,Ⅱ中反应物的转化率![]() ,转化率
,转化率![]() ,A错误;
,A错误;
B、平衡时,Ⅰ中正反应的平衡常数K(Ⅰ)![]() ,Ⅱ中正反应的平衡常数K(Ⅱ)
,Ⅱ中正反应的平衡常数K(Ⅱ)![]() ,二者互为倒数关系,B错误;
,二者互为倒数关系,B错误;
C、平衡后,Ⅰ中加入![]() 的
的![]() ,可看成原起始时体积减小一半,压强增大,
,可看成原起始时体积减小一半,压强增大,![]() 逆向移动,达到新平衡时,反应物的转化率
逆向移动,达到新平衡时,反应物的转化率![]() 减小,C错误;
减小,C错误;
D、由![]() 可知,焓变为负,为放热反应,升高温度平衡逆向移动,
可知,焓变为负,为放热反应,升高温度平衡逆向移动,![]() 均增大,则升高温度,Ⅰ、Ⅱ中气体颜色都将变深,D正确;
均增大,则升高温度,Ⅰ、Ⅱ中气体颜色都将变深,D正确;
故选D。

练习册系列答案
相关题目
【题目】在温度、容积相同的三个密闭容器中发生反应N2(g) + 3H2(g)![]() 2NH3(g) ΔH= -92.4kJ/mol,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
2NH3(g) ΔH= -92.4kJ/mol,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
容器 | 甲 | 乙 | 丙 |
反应物投入量 | 1molN2、3molH2 | 2molNH3 | 4molNH3 |
NH3的浓度(mol/L) | c1 | c2 | c3 |
反应的能量变化 | 放出a kJ | 吸收b kJ | 吸收c kJ |
体系压强 | P1 | P2 | P3 |
反应物转化率 | α1 | α2 | α3 |
下列说法正确的是
A. 2 c1>c3 B. a + b=92.4 C. 2P1<P3 D. α1 +α3=1


