题目内容
【题目】下列关于各图像的解释或结论不正确的是( )
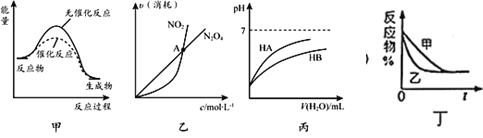
A.由甲可知:使用催化剂不影响反应热
B.由乙可知:对于恒温恒容条件下的反应![]() ,A点为平衡状态
,A点为平衡状态
C.由丙可知:等浓度的HA溶液和HB溶液,其pH前者小于后者
D.图丁表示压强对可逆反应![]() 的影响(横坐标代表时间),乙的压强比甲的压强大
的影响(横坐标代表时间),乙的压强比甲的压强大
【答案】B
【解析】
A.催化剂改变反应速率不改变化学平衡,反应热不变;
B.化学方程式可知二氧化氮和四氧化二氮反应速率之比等于化学方程式计量数之比为2:1,化学平衡状态需要正逆反应速率相同;
C.加入水稀释相同倍数,HA酸溶液PH增大的多,说明HA酸性大于HB,酸越弱溶液的pH越大;
D.对反应前后气体体积不变的反应,加压后反应速度加快,但平衡不移动;
A.催化剂能降低反应的活化能,加快反应速率化学平衡不变,反应的反应热不变,故A正确;
B.对于恒温恒容条件下的反应2NO2(g)![]() N2O4(g),图象中的A点是二氧化氮和四氧化二氮的消耗速率相同,但不能说明正逆反应速率相同,只有二氧化氮消耗速率为四氧化二氮消耗速率的二倍时才能说明反应达到平衡状态,故B错误;
N2O4(g),图象中的A点是二氧化氮和四氧化二氮的消耗速率相同,但不能说明正逆反应速率相同,只有二氧化氮消耗速率为四氧化二氮消耗速率的二倍时才能说明反应达到平衡状态,故B错误;
C.图象分析可知加入水稀释相同倍数,HA酸溶液PH增大的多,说明HA酸性大于HB,酸越弱溶液的pH越大,其pH前者小于后者,故C正确;
D.对反应前后气体体积不变的反应,加压后反应速度加快,但平衡不移动,由图乙的反应速度快,乙的压强比甲的压强大,故D正确;
故选B。

【题目】在![]() 时,将
时,将![]() 、
、![]() 分别充入两个各为
分别充入两个各为![]() 的密闭容器中,反应过程中浓度变化如下:
的密闭容器中,反应过程中浓度变化如下:![]() ,下列说法正确的是
,下列说法正确的是![]()
容器 | 物质 | 起始浓度 | 平衡浓度 |
Ⅰ |
|
|
|
| 0 |
| |
Ⅱ |
| 0 |
|
|
|
|
A.平衡时,Ⅰ、Ⅱ中反应物的转化率![]()
B.平衡时,Ⅰ、Ⅱ中上述正反应的平衡常数![]() Ⅰ
Ⅰ![]() Ⅱ
Ⅱ![]()
C.平衡后,Ⅰ中加入![]() 的
的![]() ,达到新平衡时,反应物的转化率
,达到新平衡时,反应物的转化率![]() 增大
增大
D.平衡后,升高温度,Ⅰ、Ⅱ中气体颜色都将变深