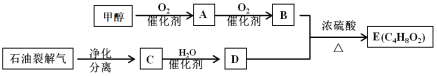
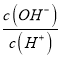题目内容
【题目】已知X、Y、Z都是短周期的元素,它们的原子序数依次递增,X原子的电子层数与它的核外电子总数相同,而Z原子的最外层电子数是次外层的三倍,Y和Z可以形成两种以上气态化合物,则:
(1)X是______,Y是______,Z是______(填元素符号)
(2)由Y和Z组成,且Y和Z的质量比为7∶20的化合物的化学式(分子式)是______.
(3)由X、Y、Z中的两种元素组成,且与![]() 分子具有相同电子数的两种离子是______和______
分子具有相同电子数的两种离子是______和______
(4)X、Y、Z可以形成一种盐,此盐中X、Y、Z元素的原子的个数比为4∶2∶3,该盐的化学式(分子式)是______
【答案】H N O ![]()
![]()
![]()
![]()
【解析】
由X、Y、Z都是短周期的元素,这三种元素的原子序数小于等于18;X原子的电子层数与它的核外电子总数相同,X是H元素;Z原子的最外层电子数是次外层的三倍,Z是O元素;X、Y、Z的原子序数依次递增,Y和Z可以形成两种以上气态化合物,知Y是N元素,据此分析解答。
(1)根据上述分析,X、Y、Z分别是H、N、O,故答案为:H、N、O;
(2)Y和Z的质量比为7∶20,其原子个数比为![]() ∶
∶![]() =2∶5,O元素的电负性大于N元素的电负性,该化合物中氮元素显正价,氧元素显负价,化学式为N2O5,故答案为:N2O5;
=2∶5,O元素的电负性大于N元素的电负性,该化合物中氮元素显正价,氧元素显负价,化学式为N2O5,故答案为:N2O5;
(3)X2Z的化学式为H2O,该分子有10个电子,由X、Y、Z中的两种元素组成,有10个电子的离子有:OH-和NH4+,故答案为:OH-;NH4+
(4)X、Y、Z可以形成一种盐,且这三种元素都是非金属元素,所以阳离子只能是NH4+,此盐中X、Y、Z元素的原子的个数比为4∶2∶3,所以酸根是NO3-,所以该盐的化学式是NH4NO3,故答案为:NH4NO3。

 阅读快车系列答案
阅读快车系列答案【题目】某铬盐厂净化含Cr(Ⅵ)废水并提取Cr2O3的一种工艺流程如图所示。
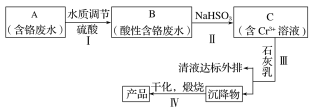
已知:Ksp[Cr(OH)3]=6.3×10-31
Ksp[Fe(OH)3]=2.6×10-39
Ksp[Fe(OH)2]=4.9×10-17
(1)步骤Ⅰ中,发生的反应为2H++2CrO42-![]() Cr2O72-+H2O,B中含铬元素的离子有___(填离子符号)。
Cr2O72-+H2O,B中含铬元素的离子有___(填离子符号)。
(2)当清液中Cr3+的浓度≤1.5mg·L-1时,可认为已达铬的排放标准。若测得清液的pH=5,则清液尚不符合铬的排放标准,因为此时Cr3+的浓度=__mg·L-1。
(3)步骤Ⅱ还可用其他物质代替NaHSO3作还原剂。
①若用FeSO4·7H2O作还原剂,步骤Ⅲ中参加反应的阳离子一定有__(填离子符号)。
②若用铁屑作还原剂,当铁的投放量相同时,经计算,C溶液的pH与c(Cr2O72-)的对应关系如下表所示:
pH | 3 | 4 | 5 | 6 |
c(Cr2O72-)/mol·L-1 | 7.02×10-21 | 7.02×10-7 | 1.25×10-3 | 2.21×10-34 |
有人认为pH=6时,c(Cr2O72-)变小的原因是Cr2O72-基本上都已转化为Cr3+。这种说法是否正确,为什么?___。
③用铁屑作还原剂时,为使所得产品中含铁元素杂质的含量尽可能低,需要控制的条件有___。
【题目】在![]() 时,将
时,将![]() 、
、![]() 分别充入两个各为
分别充入两个各为![]() 的密闭容器中,反应过程中浓度变化如下:
的密闭容器中,反应过程中浓度变化如下:![]() ,下列说法正确的是
,下列说法正确的是![]()
容器 | 物质 | 起始浓度 | 平衡浓度 |
Ⅰ |
|
|
|
| 0 |
| |
Ⅱ |
| 0 |
|
|
|
|
A.平衡时,Ⅰ、Ⅱ中反应物的转化率![]()
B.平衡时,Ⅰ、Ⅱ中上述正反应的平衡常数![]() Ⅰ
Ⅰ![]() Ⅱ
Ⅱ![]()
C.平衡后,Ⅰ中加入![]() 的
的![]() ,达到新平衡时,反应物的转化率
,达到新平衡时,反应物的转化率![]() 增大
增大
D.平衡后,升高温度,Ⅰ、Ⅱ中气体颜色都将变深