题目内容
8.下列叙述正确的是( )| A. | 0.1mol/L CH3COONa溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) | |
| B. | Na2CO3溶液加水稀释后,恢复至原温度,pH增大和KW不变 | |
| C. | 一定温度下,pH=6的HCl溶液和pH=6的NH4Cl溶液中,c(H+)相等 | |
| D. | 在Na2S溶液中加入AgCl固体,溶液中c(S2-)不变化 |
分析 A.CH3COONa溶液显碱性;
B.溶液稀释浓度减小,pH减小;
C.一定温度下,根据c(H+)=10-pH计算;
D.溶解度小的沉淀能转化为溶解度更小的.
解答 解:A.CH3COONa溶液显碱性,则0.1mol/L CH3COONa溶液:c(Na+)>c(CH3COO-)>c(OH-)>c(H+),故A错误;
B.Na2CO3溶液显碱性,加水稀释后溶液浓度减小,pH减小,Kw不变,故B错误;
C.一定温度下,c(H+)=10-pH,则pH=6的HCl溶液和pH=6的NH4Cl溶液中,c(H+)相等为10-6mol/L,故C正确;
D.溶解度小的沉淀能转化为溶解度更小的,所以在Na2S溶液中加入AgCl固体,会生成Ag2S沉淀,则溶液中c(S2-)减小,故D错误.
故选C.
点评 本题考查了盐类水解、Kw、沉淀的转化等,注意把握盐类水解的规律和溶液酸碱性的判断,为解答该题的关键,题目难度中等.

练习册系列答案
相关题目
18.某原电池装置如图所示,电池总反应为2Ag+Cl2=2AgCl,下列说法正确的是( )
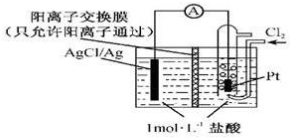

| A. | 当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少0.02 mol离子 | |
| B. | 放电时,交换膜右侧溶液中有大量白色沉淀生成 | |
| C. | 正极反应为Ag-e-=Ag+ | |
| D. | 用KCl溶液代替盐酸,则电池总反应随之改变 |
19.下列有关苯的结构与性质说法正确的是( )
| A. | 苯易溶于水 | |
| B. | 苯分子中含有碳碳双键和碳碳单键 | |
| C. | 苯能使溴水和酸性高锰酸钾溶液褪色 | |
| D. | 苯在一定条件下能发生取代反应和加成反应 |
3.NA代表阿伏伽德罗常数的值.下列叙述正确的是( )
| A. | 60g丙醇中存在的共价键总数为10NA | |
| B. | 2.0gH218O与D2O的混合物中所含中子数为NA | |
| C. | 标准状况下,5.6LCO2与足量Na2O2反应转移的电子数为0.5NA | |
| D. | 常温常压下,78g苯中含有碳碳双键的数目为3NA |
20.把体积相同,c(H+)相同的两份酸溶液,甲为盐酸,乙为醋酸,分别与锌反应,若反应后放出氢气一样多,有一份中锌有剩余,以下判断正确的是( )
①反应所需时间乙>甲
②开始反应速率甲>乙
③参加反应的锌的质量甲=乙
④整个阶段平均反应速率乙>甲
⑤盛盐酸溶液中锌有剩余
⑥盛醋酸的锌有剩余.
①反应所需时间乙>甲
②开始反应速率甲>乙
③参加反应的锌的质量甲=乙
④整个阶段平均反应速率乙>甲
⑤盛盐酸溶液中锌有剩余
⑥盛醋酸的锌有剩余.
| A. | ①②③ | B. | ①③⑥ | C. | ②③⑥ | D. | ③④⑤ |
2.恒温下用惰性电极电解某pH=a的溶液一段时间后,测知溶液的pH没发生改变,则该电解质可能是( )
| A. | NaCl溶液 | B. | AgNO3溶液 | C. | HCl溶液 | D. | 稀Na2SO4溶液 |
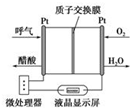 酒后驾车已成为一个社会问题.2013年1月1日起执行的新交通法规对酒后驾车作出严厉的处罚规定,检测驾驶人员呼气中酒精浓度(BrAC)的方法有多种.
酒后驾车已成为一个社会问题.2013年1月1日起执行的新交通法规对酒后驾车作出严厉的处罚规定,检测驾驶人员呼气中酒精浓度(BrAC)的方法有多种.