题目内容
20.把体积相同,c(H+)相同的两份酸溶液,甲为盐酸,乙为醋酸,分别与锌反应,若反应后放出氢气一样多,有一份中锌有剩余,以下判断正确的是( )①反应所需时间乙>甲
②开始反应速率甲>乙
③参加反应的锌的质量甲=乙
④整个阶段平均反应速率乙>甲
⑤盛盐酸溶液中锌有剩余
⑥盛醋酸的锌有剩余.
| A. | ①②③ | B. | ①③⑥ | C. | ②③⑥ | D. | ③④⑤ |
分析 醋酸是弱电解质,溶液中存在电离平衡,若c(H+)相同的醋酸和盐酸,醋酸浓度大于盐酸,等浓度等体积的醋酸和盐酸,n(CH3COOH)>n(HCl),反应速率与氢离子浓度成正比,氢离子浓度越大反应速率越快,则反应时间越短,生成氢气的质量相等,根据氢气和锌之间的关系式知,需要锌的物质的量相等.
解答 解:①若c(H+)相同的醋酸和盐酸,醋酸是弱电解质,随着反应的进行醋酸不断电离出氢离子,氯化氢完全电离,所以反应过程中,醋酸中氢离子始终大于盐酸,则醋酸反应速率大于盐酸,所以醋酸反应所需要的时间小于盐酸,故错误;
②两种溶液中氢离子浓度相等,所以开始时两种溶液反应速率相等,故错误;
③根据氢气和锌之间的关系式知,生成相同质量的氢气需要的锌的质量相等,故正确;
④根据①知,反应过程中醋酸平均反应速率大于盐酸,故正确;
⑤氢离子浓度、体积相同的醋酸和盐酸,醋酸的物质的量大于盐酸,所以盐酸中锌有剩余,故正确;
⑥根据⑤知,醋酸过量,则醋酸有剩余,锌完全反应,故错误;
故选D.
点评 本题考查了强弱电解质的电离,明确弱电解质电离特点是解本题关键,结合氢离子浓度与反应速率的关系来分析解答,难度中等.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
10.下列离子组能大量共存的是( )
| A. | K+、H+、SO42-、OH- | B. | Na+、Mg2+、OH-、NO3- | ||
| C. | Na+、H+、CO32-、Fe2+ | D. | Mg2+、Cu2+、Cl-、SO42- |
8.下列叙述正确的是( )
| A. | 0.1mol/L CH3COONa溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) | |
| B. | Na2CO3溶液加水稀释后,恢复至原温度,pH增大和KW不变 | |
| C. | 一定温度下,pH=6的HCl溶液和pH=6的NH4Cl溶液中,c(H+)相等 | |
| D. | 在Na2S溶液中加入AgCl固体,溶液中c(S2-)不变化 |
15.下列热化学方程式表述正确的是(△H的绝对值均正确)( )
| A. | NaOH(aq)+HNO3(aq)═NaNO3(aq)+H2O(l)△H=+57.3kJ/mol(中和热) | |
| B. | C2H5OH(l)+3O2(g)═2CO2(g)+3H2O(g)△H=-1367.0kJ/mol(燃烧热) | |
| C. | S(s)+O2(g)═SO2(g)△H=-269.8kJ/mol(反应热) | |
| D. | 2NO2═O2+2NO△H=+116.2kJ/mol(反应热) |
12.A、B、C、D四种物质均为下列离子组成的可溶性化合物,组成这四种物质的离子(离子不能重复组合)有:
分别取四种物质进行实验,实验结果如下
①B溶液分别与C、D混合,均有白色沉淀生成;
②将A溶液逐滴滴入C溶液中,有沉淀生成,继续滴加A溶液时,沉淀减少直至完全消失;
③A与D两种固体混合加热有气体生成,该气体能使湿润的红色石蕊试液变蓝;
④用石墨电极电解B溶液,在阳极上产生一种有刺激性气味的气体.
(1)A所含的阴离子的电子式是 ,B所含的阳离子是Ba2+.
,B所含的阳离子是Ba2+.
(2)C的化学式是Al2(SO4)3,D的化学式是(NH4)2CO3.
(3)写出②中沉淀溶解的离子方程式Al(OH)3+OH-=AlO2-+2H2O.
| 阳离子 | Na+、Al3+、Ba2+、NH4+ |
| 阴离子 | Cl-、OH-、CO32-、SO42- |
①B溶液分别与C、D混合,均有白色沉淀生成;
②将A溶液逐滴滴入C溶液中,有沉淀生成,继续滴加A溶液时,沉淀减少直至完全消失;
③A与D两种固体混合加热有气体生成,该气体能使湿润的红色石蕊试液变蓝;
④用石墨电极电解B溶液,在阳极上产生一种有刺激性气味的气体.
(1)A所含的阴离子的电子式是
 ,B所含的阳离子是Ba2+.
,B所含的阳离子是Ba2+.(2)C的化学式是Al2(SO4)3,D的化学式是(NH4)2CO3.
(3)写出②中沉淀溶解的离子方程式Al(OH)3+OH-=AlO2-+2H2O.
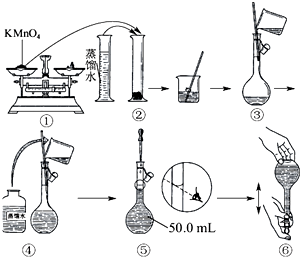 人体血液里Ca2+的浓度一般采用mg/cm3来表示.抽取一定体积的血样,加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙(CaC2O4)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得草酸(H2C2O4),再用KMnO4溶液滴定即可测定血液样品中Ca2+的浓度.某研究性学习小组设计如下实验步骤测定血液样品中Ca2+的浓度.
人体血液里Ca2+的浓度一般采用mg/cm3来表示.抽取一定体积的血样,加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙(CaC2O4)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得草酸(H2C2O4),再用KMnO4溶液滴定即可测定血液样品中Ca2+的浓度.某研究性学习小组设计如下实验步骤测定血液样品中Ca2+的浓度.
 .
.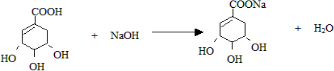 .
. -COOH),其反应类型是c
-COOH),其反应类型是c