题目内容
2.恒温下用惰性电极电解某pH=a的溶液一段时间后,测知溶液的pH没发生改变,则该电解质可能是( )| A. | NaCl溶液 | B. | AgNO3溶液 | C. | HCl溶液 | D. | 稀Na2SO4溶液 |
分析 据离子的放电顺序判断电解实质,根据电解实质判断溶液中氢离子浓度与氢氧根离子浓度的关系可知,电解后溶液的pH没发生改变,则溶液中电解本质为水,结合选项解答.
解答 解:A、电解NaCl溶液时放出氢气和氯气,则氢氧根离子的浓度增大,所以溶液的pH值增大,溶液的pH>a,故A错误;
B、电解硝酸银溶液时,阴极上析出银,阳极上得到氧气,所以溶液中的氢氧根离子的浓度减小,氢离子的浓度增大,溶液的pH值减小,溶液的pH<a,故B错误;
C、电解HCl溶液时,相当于电解HCl本身,溶液浓度减小,氢离子的浓度减小,所以溶液的pH值增大,溶液的pH>a,故C错误;
D、电解硫酸钠溶液时,实际上电解的是水,所以溶液中氢离子和氢氧根离子的相对浓度不变,只是硫酸钠的浓度增大,故pH值不变,故D正确;
故选D.
点评 本题考查了电解原理,随着电解的进行判断溶液pH值的变化,首先要知道离子的放电顺序、电解的实质,只有明白这些知识点才能正确解答.

练习册系列答案
相关题目
8.下列叙述正确的是( )
| A. | 0.1mol/L CH3COONa溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) | |
| B. | Na2CO3溶液加水稀释后,恢复至原温度,pH增大和KW不变 | |
| C. | 一定温度下,pH=6的HCl溶液和pH=6的NH4Cl溶液中,c(H+)相等 | |
| D. | 在Na2S溶液中加入AgCl固体,溶液中c(S2-)不变化 |
17.下列判断正确的是( )
| A. | T℃时,KW=1.0×10-12.该温度下,PH=3的溶液中,水电离出的c(H+)=1.0×10-11 | |
| B. | 25℃时,PH=a的氨水与PH=b的盐酸等体积混合至溶液呈中性,则a+b=14 | |
| C. | 0.1mol/LNaHCO3溶液中:c(HCO3-)>c(CO32-)>c(H2CO3) | |
| D. | 0.1mol/LCH3COOH溶液与0.05mol/LNaOH溶液等体积混合,所得溶液中,2c(H+)+c(CH3COOH)=c(CH3COO-)+2c(OH-) |
7.下列离子可能大量共存的是( )
| A. | 无色溶液:Al3+、NH4+、Cl?、S2? | |
| B. | 酸性溶液:Na+、ClO?、SO42?、I? | |
| C. | 0.1mol/LFeCl3溶液中:Fe2+、NH4+、SCN-、SO42- | |
| D. | 常温下,水电离出的c(H+)=1×10-13 mol•L-1的溶液:K+、Na+、Cl-、S2- |
11.下列离子方程式正确的是( )
| A. | 向FeSO4溶液中加入少量Na2O2:4Na2O2+6H2O+4Fe2+═4Fe(OH)3↓+8Na++O2↑ | |
| B. | 向明矾溶液中逐滴加入Ba(OH)2溶液至沉淀的质量最大:2Al3++3SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓ | |
| C. | 向NaClO溶液中通入少量SO2: 2ClO-+SO2+H2O═2HClO+SO32- | |
| D. | 将0.2 mol/L的NH4Al(SO4)2溶液与0.4 mol/L的Ba(OH)2溶液等体积混合:NH4++Al3++2SO42-+2Ba2++4OH-═Al(OH)3↓+2BaSO4↓+NH3•H2O |
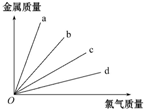 如图所示,钠、镁、铝、铁分别跟足量的氯气反应时,消耗金属的质量与反应的氯气的质量之间的关系,其中表示铝与氯气反应的是( )
如图所示,钠、镁、铝、铁分别跟足量的氯气反应时,消耗金属的质量与反应的氯气的质量之间的关系,其中表示铝与氯气反应的是( )