��Ŀ����
����Ŀ������ʵ�������Ԥ��ʵ��Ŀ�Ļ�����ʵ�����һ�µ���
ѡ�� | ʵ����������� | Ԥ��ʵ��Ŀ�Ļ���� |
A | �ýྻ�IJ�˿պȡijʳ���������ھƾ��ƻ��������գ������Ի�ɫ | ˵����ʳ�β��Ǽӵ��� |
B | ������Һ�е����������ΪC2H4O2��Һ̬�л��ˮԡ�ȣ����������� | ��ȷ�����л���һ���Ǽ������ |
C | ����֧ʢ��KI3����Һ���Թ��У��ֱ�μӵ�����Һ��AgNO3��Һ��ǰ����Һ�����������л�ɫ���� | KI3��Һ�д���ƽ�⣺I3-=I2+I- |
D | Ũ�������Ҵ�170�湲�ȣ��Ƶõ�����ͨ�����Ը��������Һ����Һ��ɫ��ȥ | �Ƶõ��������Ϊ��ϩ |
A. A B. B C. C D. D
���𰸡�C
��������A���ص���ɫ��Ӧ�ܱ��Ƶ���ɫ��Ӧ���ڸǣ��۲�ص���ɫ��ӦҪ����ɫ�ܲ��������ʵ���в���ȷ���Ƿ�KIO3��ѡ��A����B��������Һ�е����������ΪC2H4O2��Һ̬�л��ˮԡ�ȣ����������֣�һ����-CHO������ΪHOCH2CHO����������ѡ��B����C������֧ʢ��KI3����Һ���Թ��У��ֱ�μӵ�����Һ��AgNO3��Һ��ǰ����Һ�����������л�ɫ��������KI3����Һ�к�I2��I-����KI3��Һ�д���ƽ��ΪI3-![]() I2+I-��ѡ��C��ȷ��D���Ҵ��ӷ�����ϩ�л����Ҵ������߾��ܱ���������Ӧ�ȳ�ȥ�Ҵ�����ͨ�����Ը��������Һ���۲쵽��Һ��ɫ�ܿ���ȥ��֤����Ӧ��������ϩ��ѡ��D����ѡC��
I2+I-��ѡ��C��ȷ��D���Ҵ��ӷ�����ϩ�л����Ҵ������߾��ܱ���������Ӧ�ȳ�ȥ�Ҵ�����ͨ�����Ը��������Һ���۲쵽��Һ��ɫ�ܿ���ȥ��֤����Ӧ��������ϩ��ѡ��D����ѡC��

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�����Ŀ��X��Y��Z��M��Q��R��6�ֶ�����Ԫ�أ���ԭ�Ӱ뾶����Ҫ���ϼ����±���ʾ��
Ԫ�ش��� | X | Y | Z | M | Q | R |
ԭ�Ӱ뾶/nm | 0.160 | 0.143 | 0.102 | 0.075 | 0.077 | 0.037 |
��Ҫ���ϼ� | ��2 | ��3 | ��6����2 | ��5����3 | ��4����4 | ��1 |
(1)����ͭ��Ԫ��M������������Ӧ��ˮ�����ϡ��Һ������Ӧ�����ӷ���ʽΪ________________________________________________________________________��
(2)Ԫ��Q��Ԫ��Z�ĺ���Ӱ��������ܣ�������ͼװ��A�ڸ����½�������Ԫ��Q��Ԫ��Zת��ΪQO2��ZO2��
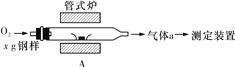
������a�ijɷ���________________(�ѧʽ)��
����������Ԫ��Z��FeZ����ʽ���ڣ���װ��A�з�Ӧ����ZO2���ȶ��ĺ�ɫ�������Ӧ�Ļ�ѧ����ʽ�ǣ�______________________________________________��
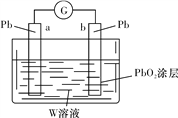
(3)��Z����ۺ�����W����Һ���������Һ(���Ϊ1 L�����跴Ӧǰ����Һ����仯���Բ���)��װ��ԭ���(��ͼ��ʾ)������a�缫�Ϸ����ķ�Ӧ�ɱ�ʾΪ_________________������ع���һ��ʱ���a������0.05 mol Pb����W��Һ��Ũ������������39%(�ܶ�Ϊ1.3 g/cm3)��Ϊ______mol/L(����һλС��)��
����Ŀ���±���Ԫ�����ڱ���һ���֣���ش��й����⣺
������ ���ڡ��� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0 |
2 | �� | �� | �� | |||||
3 | �� | �� | �� | �� | �� | |||
4 | �� | �� |
(1)���л�ѧ��������õ�Ԫ�أ���ԭ�ӽṹʾ��ͼΪ__________��
(2)����Ԫ�����ڱ��е�λ����_______________________________��
(3)�õ���ʽ��ʾ����ߵ�ԭ���γɻ�����Ĺ��̣�_________________________________��
(4)����������֤�ܢ�����Ԫ�ؽ�����ǿ����ʵ����__________(����ĸ����)��
a�����ڿ����з����Ѿõ�������Ԫ�صĿ�״���ʷֱ����ˮ��
b������״����С��ͬ��������Ԫ�صĵ��ʷֱ��ͬŨ�ȵ����ᷴӦ
c������״����С��ͬ��������Ԫ�صĵ��ʷֱ���¶���ͬ����ˮ���ã��������̪
d���Ƚ�������Ԫ�ص��⻯����ȶ���
(5)�ޢ�����Ԫ�صļ������ӻ�ԭ�Խ�ǿ����________(�����ӷ���)����һ���û���Ӧ֤ʵ��һ����__________________________(�ѧ����ʽ)��

