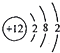
��Ŀ����
����Ŀ���й����ʵ�ת����ϵ��ͼ��ʾ��������������������ȥ����A��C��E��G�� ��ѧ��ѧ�г����ĵ��ʣ�ͨ��״���£�E���ܶ���С�����壬G�ǻ���ɫ�����壬B �dz�������ɫҺ�壬FΪǿ�D��ij�־��д��ԵĽ����������Ҫ�ɷ֣�K���ȷֽ�����ɺ���ɫ���壮 
��ش��������⣺
��1��D�Ļ�ѧʽΪ
��2��H�ĵ���ʽΪ
��3��д��A��B��Ӧ�Ļ�ѧ����ʽ��
��4��д��������G��F����Һ��Ӧ�����ӷ���ʽ�� ��
���𰸡�
��1��Fe3O4
��2��![]()
��3��2Na+2H2O=2NaOH+H2��
��4��Cl2+2OH��=Cl��+ClO��+H2O
���������⣺A��C��E��G����ѧ��ѧ�г����ĵ��ʣ�ͨ��״���£�E���ܶ���С�����壬��EΪH2 �� G�ǻ���ɫ�����壬��GΪCl2 �� E��G��Ӧ����HΪHCl��B �dz�������ɫҺ�壬FΪǿ���AΪNa��BΪH2O��FΪNaOH��D��ij�־��д��ԵĽ����������Ҫ�ɷ֣�K���ȷֽ�����ɺ���ɫ���壬K��Ӧ�õ�I����CΪFe��DΪFe3O4 �� ������������������Ӧ�����Ȼ��������Ȼ�������I����Fe��Ӧ�õ�G��G��������Ӧ�õ�I����IΪFeCl3��GΪFeCl2 �� KΪFe��OH��3 �� ����ת����ϵ��
��1.��D�Ļ�ѧʽΪFe3O4 �� �ʴ�Ϊ��Fe3O4��
��2.��HΪHCl������ʽΪ ![]() ���ʴ�Ϊ��
���ʴ�Ϊ�� ![]() ��
��
��3.��A��B��Ӧ�Ļ�ѧ����ʽ��2Na+2H2O=2NaOH+H2�����ʴ�Ϊ��2Na+2H2O=2NaOH+H2����
��4.������������������������Һ��Ӧ�����ӷ���ʽ��Cl2+2OH��=Cl��+ClO��+H2O���ʴ�Ϊ��Cl2+2OH��=Cl��+ClO��+H2O��
A��C��E��G����ѧ��ѧ�г����ĵ��ʣ�ͨ��״���£�E���ܶ���С�����壬��EΪH2 �� G�ǻ���ɫ�����壬��GΪCl2 �� E��G��Ӧ����HΪHCl��B �dz�������ɫҺ�壬FΪǿ���AΪNa��BΪH2O��FΪNaOH��D��ij�־��д��ԵĽ����������Ҫ�ɷ֣�K���ȷֽ�����ɺ���ɫ���壬K��Ӧ�õ�I����CΪFe��DΪFe3O4 �� ������������������Ӧ�����Ȼ��������Ȼ�������I����Fe��Ӧ�õ�G��G��������Ӧ�õ�I����IΪFeCl3��GΪFeCl2 �� KΪFe��OH��3 ��

����Ŀ������ʵ�������Ԥ��ʵ��Ŀ�Ļ�����ʵ�����һ�µ���
ѡ�� | ʵ����������� | Ԥ��ʵ��Ŀ�Ļ���� |
A | �ýྻ�IJ�˿պȡijʳ���������ھƾ��ƻ��������գ������Ի�ɫ | ˵����ʳ�β��Ǽӵ��� |
B | ������Һ�е����������ΪC2H4O2��Һ̬�л��ˮԡ�ȣ����������� | ��ȷ�����л���һ���Ǽ������ |
C | ����֧ʢ��KI3����Һ���Թ��У��ֱ�μӵ�����Һ��AgNO3��Һ��ǰ����Һ�����������л�ɫ���� | KI3��Һ�д���ƽ�⣺I3-=I2+I- |
D | Ũ�������Ҵ�170�湲�ȣ��Ƶõ�����ͨ�����Ը��������Һ����Һ��ɫ��ȥ | �Ƶõ��������Ϊ��ϩ |
A. A B. B C. C D. D