题目内容
化学与能源开发,环境保护、生产生活等密切相关.下列有关说法正确的是( )
| A、二氧化硫可用于纸浆漂白,表明二氧化硫具有还原性 |
| B、CO、NO、NO2都是大气污染气体,在空气中都能稳定存在 |
| C、明矾可用于净水是因为它能够消毒杀菌 |
| D、静电除尘、血液透析均与胶体性质相关 |
考点:常见的生活环境的污染及治理,胶体的重要性质,盐类水解的应用
专题:化学应用
分析:A.二氧化硫有漂白性,能漂白某些物质;
B.NO能与氧气反应生成NO2;
C.明矾净水原理是电离出的铝离子水解生成氢氧化铝胶体具有吸附性;
D.静电除尘是利用胶体电泳性质的应用,血液透析原理即为胶体渗析原理;
B.NO能与氧气反应生成NO2;
C.明矾净水原理是电离出的铝离子水解生成氢氧化铝胶体具有吸附性;
D.静电除尘是利用胶体电泳性质的应用,血液透析原理即为胶体渗析原理;
解答:
解:A.二氧化硫可用于纸浆漂白,表明二氧化硫具有漂白性,故A错误;
B.CO、NO、NO2都是大气污染气体,CO、NO2在空气中都能稳定存在,NO能与氧气反应生成NO2,故B错误;
C.明矾净水原理是硫酸铝钾溶液中含有铝离子,铝离子水解Al3++3H2O?Al(OH)3(胶体)+3H+,生成氢氧化铝胶体和氢离子,氢氧化铝胶体具有吸附性净水,不能消毒杀菌,故C错误;
D.静电除尘是利用胶体电泳性质的应用,血液透析原理即为胶体渗析原理,均与胶体性质相关,故D正确;
故选D.
B.CO、NO、NO2都是大气污染气体,CO、NO2在空气中都能稳定存在,NO能与氧气反应生成NO2,故B错误;
C.明矾净水原理是硫酸铝钾溶液中含有铝离子,铝离子水解Al3++3H2O?Al(OH)3(胶体)+3H+,生成氢氧化铝胶体和氢离子,氢氧化铝胶体具有吸附性净水,不能消毒杀菌,故C错误;
D.静电除尘是利用胶体电泳性质的应用,血液透析原理即为胶体渗析原理,均与胶体性质相关,故D正确;
故选D.
点评:本题考查生活中化学反应原理,涉及物质的性质与用途,有利于培养学生的良好的科学素养,提高学习的积极性,难度不大,注意相关基础知识的积累.

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案
相关题目
下列关于元素化合价的叙述错误的是( )
| A、ⅢA族的B和Al都能形成+3价的化合物 |
| B、ⅣA族的C和Si都能形成+4价的化合物 |
| C、VA族的N和P都能形成+5价的化合物 |
| D、ⅥA族的O和S都能形成+6价的化合物 |
关于卤素(用X表示)的下列叙述正确的是( )
| A、卤素单质与水反应均可用X2+H2O═HXO+HX表示 |
| B、由于Cl的非金属性比Br强,故盐酸的酸性比氢溴酸的酸性强 |
| C、卤素单质的密度从F2→I2随相对分子质量增大而增大 |
| D、F2可以从NaCl溶液中置换出Cl2 |
下列说法不正确的是( )
| A、“地沟油”经加工处理后,可用来制肥皂和生物柴油,可以实现厨余废物合理利用 |
| B、蔗糖、淀粉、油脂及其水解产物中既有电解质也有非电解质 |
| C、分光光度计可用于某些化学反应速率的实验测定 |
| D、分子间作用力比化学键弱得多,但它对物质溶解度影响较大,对熔点、沸点无影响 |
乙醇汽油是被广泛使用的新型清洁燃料,工业生产乙醇的一种反应原理为:2CO2(g)+6H2(g)?CH3CH2OH(g)+3H2O(g).下列有关说法正确的是( )
| A、升高温度,平衡逆向移动,说明此反应△H<0 |
| B、H2O分子间不存在氢键 |
| C、CH3CH2OH分子中α键和π键个数比为1:1 |
| D、每生成1mol乙醇转移电子6mol |
在硫酸的工业制法中,下列生产操作及说明生产操作的主要原因二者都正确的是( )
| A、从沸腾炉出来的炉气需净化,因为炉气中SO3会与杂质反应 |
| B、硫铁矿燃烧前需要粉碎,因为大块的不能燃烧 |
| C、SO3用98.3%的浓硫酸吸收,目的是防止形成酸雾,以便使SO3吸收完全 |
| D、SO2氧化为SO3时需要使用催化剂,这样可以提高SO2的转化率 |
下列叙述中正确的是( )
| A、一切四面体空间构型的分子内键角均为109°28′ |
| B、Cu(OH)2能溶于过量氨水形成络合物[Cu(NH3)4]2+,中心离子为Cu2+,配位体是NH3 |
| C、任何晶体,若含阳离子也一定含阴离子 |
| D、水分子稳定是因为水分子间存在氢键作用 |
下列各组微粒,按半径由大到小的顺序排列的是( )
| A、Mg、Ca、K、Na |
| B、S2-、Cl-、K+、Ca2+ |
| C、Br-、Br、Cl、S |
| D、Na+、Al3+、Cl-、F- |
下列图示与对应的叙述相符合的是( )
A、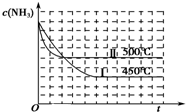 N2(g)+3H2?2NH3(g)△H<0 |
B、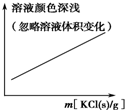 FeCl3+3KSCN?Fe(SCN)3+3KCl |
C、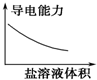 向稀醋酸中加入醋酸钠溶液 |
D、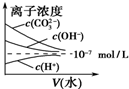 稀释苏打溶液 |