题目内容
17.NA代表阿伏加德罗常数的值,下列说法正确的是( )| A. | 常温常压,11.2 L NO和O2混合气体的原子数为NA | |
| B. | 1.5 g甲基所含有的电子数目为0.9NA | |
| C. | 1 L 0.1mol/L的氨水中含有的N原子数小于0.1NA | |
| D. | 7.8g苯中碳碳双键的数目为0.3NA |
分析 A、在标准状况下气体摩尔体积为22.4L/mol;
B、根据n=$\frac{m}{M}$和甲基(-CH3)所含的电子数来计算;
C、依据一水合氨是弱电解质,溶液中氮元素守恒分析判断;
D、苯分子中的碳碳键为一种介于单键和双键之间的独特键,不存在碳碳双键.
解答 解:A、在标准状况下气体摩尔体积为22.4L/mol,常温常压,11.2 L NO和O2混合气体物质的量不是0.5mol,故A错误;
B、15g甲基(-CH3)的物质的量n=$\frac{m}{M}$=$\frac{1.5g}{15g/mol}$=0.1mol,而1mol甲基(-CH3)含9mol电子,0.1mol甲基中电子数为0.9NA,故B正确;
C、1L0.1mol/L氨水溶质物质的量为0.1mol,1 L 0.1mol/L的氨水中含有的N原子数等于0.1NA,故C错误;
D、7.8g苯的物质的量为0.1mol,苯分子中的碳碳键为一种独特键,其分子中不存在碳碳双键,故D错误;
故选B.
点评 本题是以阿伏伽德罗常数为载体综合考查物质的结构、性质及反应原理等知识点,考查阿伏伽德罗常数与微粒数的关系,题目较简单.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.下列说法正确的是( )
| A. | 按系统命名法,化合 的名称为2-甲基-3-乙基丁烷 的名称为2-甲基-3-乙基丁烷 | |
| B. | 甲醇、乙醇、甘油互为同系物 | |
| C. | 等物质的量的乙炔、乙醛,完全燃烧时的耗氧量不相等 | |
| D. | 以乙烯为原料制备乙酸乙酯的合成路线可以为: |
8.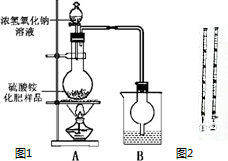 利用硫酸工业尾气中的二氧化硫可以制取氮肥硫酸铵.某探究小组设计实验对制得硫酸铵的品质进行鉴定.
利用硫酸工业尾气中的二氧化硫可以制取氮肥硫酸铵.某探究小组设计实验对制得硫酸铵的品质进行鉴定.
【查阅资料】硫酸铵化肥品质的束腰指标如表:
【观察外观】该硫酸铵化肥无可见机械杂质.
实验一:气体法测定含氮量.(实验装置如图1所示)
(1)烧瓶内发生反应的离子方程式为:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O;烧杯中盛放的试剂最好是稀硫酸(填“浓硫酸”、“稀硫酸”或“水”)
(2)甲同认为根据此实验测得的数据,计算硫酸铵化肥的含氮量可能偏高,因为实验装置中存在一个明显缺陷是:A、B装置间缺一个干燥装置.针对甲同学指出的缺陷,他们改进了实验装置,重新进行实验,准确测得氢气的质量.
实验二:甲醛法测定含氮量.
已知:①甲醛结构简式为HCHO,在空气中易被氧化成甲酸,甲酸酸性比乙醛强.
②甲醛法的反应原理为:4NH4++6HCHO→4H++6H2O+(CH2)6N4生成的酸再用NaOH标准溶液滴定,从而测定氮的含量.
(1)实验步骤:称取固体(NH4)2SO4样品0.600g于烧杯中,加入约30mL蒸馏水溶解,最终配成100mL溶液,用②(填图2中仪器编号)滴定管准确取出20.00mL的溶液与锥形瓶中,加入18%中性甲醛溶液5mL,放置5min后,加入1~2滴指示剂(已知滴定终点的pH约为8.8),用浓度为0.1000mol•L-1 NaOH标准溶液滴定,读数如表:
(2)探究结论,该化肥是(填“是”或“不是”)一等品.
(3)若滴定前待测也加甲醛后露置空气时间过长,则所测定的含氮量比实际值偏大(填“偏大”“偏小”或“无影响”).
实验三:测定碳酸氢铵中的含氮量
碳酸氢铵也是常用的氮肥,如果测定其含氮量,应选择的方法是气体法(填“气体法”或“甲醛法”),不选择另一种方法的理由是甲醛法用氢氧化钠标准溶液滴定时,溶液中HCO3-中的H+也会和氢氧化钠中和.
 利用硫酸工业尾气中的二氧化硫可以制取氮肥硫酸铵.某探究小组设计实验对制得硫酸铵的品质进行鉴定.
利用硫酸工业尾气中的二氧化硫可以制取氮肥硫酸铵.某探究小组设计实验对制得硫酸铵的品质进行鉴定.【查阅资料】硫酸铵化肥品质的束腰指标如表:
| 指标 项目 | 优等品 | 一等品 | 合格品 |
| 外观 | 白色结晶,无可见机械杂质 | 无可见机械杂质 | |
| 氮(N)含量 | ≥21.0% | ≥21.0% | ≥20.5% |
实验一:气体法测定含氮量.(实验装置如图1所示)
(1)烧瓶内发生反应的离子方程式为:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O;烧杯中盛放的试剂最好是稀硫酸(填“浓硫酸”、“稀硫酸”或“水”)
(2)甲同认为根据此实验测得的数据,计算硫酸铵化肥的含氮量可能偏高,因为实验装置中存在一个明显缺陷是:A、B装置间缺一个干燥装置.针对甲同学指出的缺陷,他们改进了实验装置,重新进行实验,准确测得氢气的质量.
实验二:甲醛法测定含氮量.
已知:①甲醛结构简式为HCHO,在空气中易被氧化成甲酸,甲酸酸性比乙醛强.
②甲醛法的反应原理为:4NH4++6HCHO→4H++6H2O+(CH2)6N4生成的酸再用NaOH标准溶液滴定,从而测定氮的含量.
(1)实验步骤:称取固体(NH4)2SO4样品0.600g于烧杯中,加入约30mL蒸馏水溶解,最终配成100mL溶液,用②(填图2中仪器编号)滴定管准确取出20.00mL的溶液与锥形瓶中,加入18%中性甲醛溶液5mL,放置5min后,加入1~2滴指示剂(已知滴定终点的pH约为8.8),用浓度为0.1000mol•L-1 NaOH标准溶液滴定,读数如表:
| 滴定次数 | 滴定前读数/mL | 滴定后读数/mL |
| 1 | 1.20 | 18.91 |
| 2 | 0.00 | 18.60 |
| 3 | 1.10 | 18.79 |
(3)若滴定前待测也加甲醛后露置空气时间过长,则所测定的含氮量比实际值偏大(填“偏大”“偏小”或“无影响”).
实验三:测定碳酸氢铵中的含氮量
碳酸氢铵也是常用的氮肥,如果测定其含氮量,应选择的方法是气体法(填“气体法”或“甲醛法”),不选择另一种方法的理由是甲醛法用氢氧化钠标准溶液滴定时,溶液中HCO3-中的H+也会和氢氧化钠中和.
5.一定条件下,利用如图所示装置可实现有机物的储氢,下列有关说法正确的是( )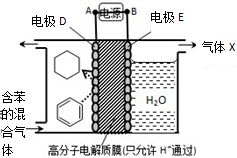

| A. | 电极D的电极反应式为C6H6+6H++6e-=C6H12 | |
| B. | 气体X在反应中通常体现还原性 | |
| C. | 电极D为惰性电极,E为活泼电极 | |
| D. | 外电路电子的移动方向:A→电极→B |
12.锂离子电池种类很多,其中有一种锂电池,用金属锂和石墨做电极材料,电解质溶液是由四氯铝锂(LiAlCl4)溶解在亚硫酰氯(SOCl2)中而形成的,电池总反应方程式为8Li+3SOCl2=6LiCl+Li2SO3+2S,则下列叙述中错误的是( )
| A. | 电解质溶液中混入水,会影响电池反应 | |
| B. | 反应中,SOCl2既是溶剂,又是氧化剂 | |
| C. | 电池工作过程中,亚硫酰氯(SOCl2) 被还原为Li2SO3 | |
| D. | 电池工作过程中,金属锂提供的电子与正极区析出硫物质的量之比为4:1 |
2.背景材料:
①浙大研制的石墨烯弹性气凝胶(又名碳海绵)入选2013年度世界最轻固体材料;
②2014年11月上旬北京APEC峰会期间,政府重拳整治雾霾,蓝天重现;
③中科大最近成功发现了一种新的铁基超导材料 (Li0.8Fe0.2)OHFeSe(Se呈-2价).
④瑞典皇家理工学院(KTH)的研究人员已经成功的构建出了一种能使水快速氧化成氧气的分子催化剂.
下列说法不正确的是( )
①浙大研制的石墨烯弹性气凝胶(又名碳海绵)入选2013年度世界最轻固体材料;
②2014年11月上旬北京APEC峰会期间,政府重拳整治雾霾,蓝天重现;
③中科大最近成功发现了一种新的铁基超导材料 (Li0.8Fe0.2)OHFeSe(Se呈-2价).
④瑞典皇家理工学院(KTH)的研究人员已经成功的构建出了一种能使水快速氧化成氧气的分子催化剂.
下列说法不正确的是( )
| A. | 石墨烯弹性气凝胶可用作处理海上原油泄漏的吸油材料 | |
| B. | 压减燃煤、严格控车、调整产业是治理雾霾的有效措施 | |
| C. | 新的铁基超导材料中Fe的化合价呈+2、+3价 | |
| D. | 该分子催化剂可将一次能源太阳能直接转化成二次能源 |
9.设NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,1.12L1H2和0.2g 2H2均含有0.1NA个质子 | |
| B. | 在同压不同温的情况下,质量相同的氧气和臭氧所含氧原子数不相同 | |
| C. | 标准状况下,11.2L庚烷完全燃烧后生成的CO2分子数为3.5NA | |
| D. | 常温下,将5.6 g 铁投入足量的浓硫酸中转移电子数为0.3 NA |
6.化学与生活密切相关,下列说法不正确的是( )
| A. | Fe2O3常用作红色油漆和涂料 | B. | 氟氯烃是安全、环保的制冷剂 | ||
| C. | 聚丙烯酸钠可做“尿不湿”原料 | D. | 硅胶可用作瓶装药品干燥剂 |
7.下列化学用语正确的是( )
| A. | 甲基的电子式是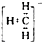 | B. | 硫的原子结构示意图是 | ||
| C. | ${\;}_{8}^{18}$O表示中子数是18的氧原子 | D. | 过氧化氢的结构式是H-O-O-H |