题目内容
【题目】“探险队员”——盐酸,不小心走进了化学迷宫,不知怎样走出来,因为迷宫有许多“吃人的野兽”(即能与盐酸反应的物质或者是水溶液),盐酸必须避开它们,否则就无法通过。
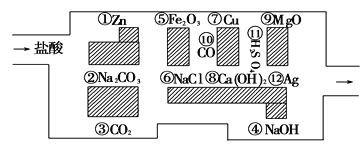
(1)迷宫内12种物质中属于碱性氧化物的有________________,写出其中一种与盐酸反应的化学方程式________________________________________。
(2)迷宫内12种物质中金属单质及其活动顺序是_________________,试写一个相互置换的化学方程式:________________________________________
【答案】⑤⑨ Fe2O3 +6HCl =2FeCl3+3H2O (或MgO) ①⑦ Zn+2HCl = ZnCl2+H2↑
【解析】
盐酸是强酸,能跟金属活动顺序表中氢位前的金属反应如Zn、Fe等,不能跟氢位后的金属如Cu、Ag等反应,盐酸能与弱酸的盐反应如Na2CO3等;盐酸能与碱性氧化物反应如Fe2O3、 MgO等;盐酸能与碱发生中和反应如NaOH、Ca(OH)2等,由此分析。
(1)能与酸反应生成盐和水的氧化物称为碱性氧化物,
Fe2O3+6HCl=2FeCl3+3H2O、MgO+2HC1=MgCl2+H2O 所以Fe2O3和MgO属于碱性氧化物,即⑤⑨属于碱性氧化物;它们与盐酸反应的离子方程式为Fe2O3+6HCl=2FeCl3+3H2O、MgO+2HC1=MgCl2+H2O;
(2)根据金属活动顺序表,越靠前的金属越活波,因此活动性由强到弱的顺序是Zn>Cu>Ag;即活动性由强到弱的顺序是①⑦;它们之间发生置换反应的化学方程式有:Zn+2HCl = ZnCl2+H2↑等。

练习册系列答案
相关题目