题目内容
【题目】请根据如图所示的实验过程和提供的数据,计算生石灰样品中钙元素的质量____________.
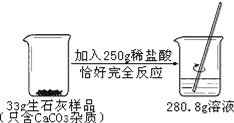
(不考虑其它因素对实验的影响,要求有计算过程)
【答案】22g
【解析】
根据反应CaCO3+2HCl═CaCl2+H2O+CO2↑中碳酸钙与二氧化碳的关系进行计算。
生成二氧化碳的质量为:33g+250g-280.8g=2.2g。
设:碳酸钙的质量为x,
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 2.2 g
![]() =
=![]()
x=5g,
样品中氧化钙的质量为:33g-5g=28g,
碳酸钙中钙元素的质量为:5g×![]() ×100%=2g,
×100%=2g,
氧化钙中钙元素质量为:28g×![]() ×100%=20g,
×100%=20g,
生石灰样品中钙元素的质量为:2g+20g=22g,
答:生石灰样品中钙元素的质量为22g。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目