题目内容
13.在一定体积的密闭容器中,进行如下反应:CO2(g)+H2(g)?CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应化学平衡常数的表达式:K=$\frac{c(CO)c({H}_{2}O)}{c(C{O}_{2})c({H}_{2})}$;
(2)该反应为吸热(填“吸热”或“放热”)反应;
(3)下列说法中能说明该反应达平衡状态的是B
A.容器中压强不变 B.混合气体中c(CO)不变
C.混合气体的密度不变 D.c(CO)=c(CO2)
E.单位时间内生成CO的分子数与生成H2O的分子数相等
(4)为了提高H2的转化率,下列措施可行的是D
A.降低温度 B.使用催化剂
C.增大压强 D.循环利用和不断补充CO2
(5)某温度下,各物质的平衡浓度符合下式:c(CO2)×c(H2)=c(CO)×c(H2O),试判此时的温度为830℃.
分析 (1)根据化学平衡常数的概念来书写,平衡常数等于生成物平衡浓度幂次方乘积除以反应物平衡浓度幂次方乘积;
(2)根据温度对化学平衡、化学平衡常数的影响来回答;
(3)化学平衡状态的标志:正逆反应速率相等,各组分含量保持不变及其衍生的物理量关系分析判断;
(4)提高H2的转化率,可以使平衡正向进行,根据化学平衡移动原理来回答判断,注意只增大H2的浓度,平衡向正反应方向移动,但H2的转化率会降低.
(5)某温度下,各物质的平衡浓度符合下式:c(CO2).c(H2)=c(CO).c(H2O),说明 K=1,由此分析解答.
解答 解:(1)因平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积,所以K=$\frac{c(CO)c({H}_{2}O)}{c(C{O}_{2})c({H}_{2})}$,故答案为:$\frac{c(CO)c({H}_{2}O)}{c(C{O}_{2})c({H}_{2})}$;
(2)化学平衡常数的大小只与温度有关,升高温度,平衡向吸热的方向移动,由表可知:升高温度,化学平衡常数增大,说明化学平衡正向移动,因此正反应方向吸热,
故答案为:吸热;
(3)A、反应是一个反应前后体积不变的反应,压强始终不变,故A错误;
B、化学平衡时,各组分的浓度不随时间的改变而改变,故B正确;
C、混合气体的密度始终不变,故C错误;
D、c(CO)=c(CO2),而不是不变,故D错误
E、单位时间内生成CO的分子数与生成H2O的分子数相等,都体现的正反应方向,未体现正与逆的关系,故E错误;
故选B;
(4)CO2(g)+H2(g)?CO(g)+H2O(g),反应是吸热反应,
A.降低温度,平衡向逆反应方向减小,氢气转化率减小,故A错误;
B.使用催化剂改变反应速率不改变化学平衡,故B错误;
C.反应前后气体体积不变,增大压强平衡不动,氢气转化率不变,故C错误;
D.两种反应物增大一种会提高另一种物质的转化率,循环利用和不断补充CO2,提高氢气转化率,故D正确;
故答案为:D.
(5)某温度下,各物质的平衡浓度符合下式:c(CO2).c(H2)=c(CO).c(H2O),说明 K=1,对应的温度是830℃,故答案为:830℃.
点评 本题考查学生化学平衡成熟的含义和表达式的书写知识,可以根据所学知识进行回答,难度不大.

 导学教程高中新课标系列答案
导学教程高中新课标系列答案| A. | 石油的裂化、油脂的硬化、煤的液化均属于化学变化 | |
| B. | 葡萄糖、蔗糖、麦芽糖均属于还原性糖 | |
| C. | 淀粉、纤维素均属于天然高分子化合物 | |
| D. | Al2O3、Al(OH)3、氨基酸均为两性化合物,能与酸、碱反应生成盐 |
| A. | 凡是含有碳元素的化合物都属于有机物 | |
| B. | 易溶于汽油、酒精、苯等有机溶剂中的物质,一定是有机物 | |
| C. | 所有的有机物都很容易燃烧 | |
| D. | 大多数有机物都是共价化合物 |
| A. | 苯和甲苯不互为同系物 | B. | 淀粉和纤维素互为同分异构体 | ||
| C. | 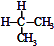 与 与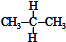 互为同分异构体 互为同分异构体 | D. | 异丁烷与2-甲基丙烷互为同种物质 |
| A. | C8H18(l)+12.5O2(g)═8CO2(g)+9H2O(g)△H=-48.40KJ/mol | |
| B. | C8H18(l)+12.5O2(g)═8CO2(g)+9H2O(l)△H=-5518KJ/mol | |
| C. | C8H18(l)+12.5O2(g)═8CO2(g)+9H2O(l)△H=+5518KJ/mol | |
| D. | C8H18(l)+12.5O2(g)═8CO2(g)+9H2O(l)△H=-48.40KJ/mol |
| A. | 苯的同系物均可被酸性KMnO4溶液氧化 | |
| B. | 苯的同系物是分子中仅含有一个苯环的烃类物质 | |
| C. | 苯不能使酸性KMnO4溶液褪色,甲苯能使酸性KMnO4溶液褪色是因为甲苯中苯环对甲基的影响 | |
| D. | 相同质量的甲烷和乙烷完全燃烧甲烷耗氧量多 |
| A. | 可用溴水鉴别苯、乙醇、1-己烯、乙酸溶液和苯酚溶液 | |
| B. | 分子式为C7H8O的芳香族化合物有5种,能与碳酸钠溶液反应的有4种 | |
| C. | 人体需要的营养素主要有:蛋白质、脂类、糖类、无机盐、维生素和水 | |
| D. | 将溴乙烷与氢氧化钠乙醇溶液共热产生的气体通入高锰酸钾酸性溶液后,溶液褪色,即证明有乙烯生成 | |
| E. | 分子式为C4H10O,能催化氧化为醛的有机物的核磁共振氢谱图有可能为2个峰 |

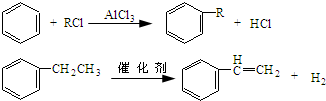
 +CH3CH2Cl$→_{△}^{AlCl_{3}}$
+CH3CH2Cl$→_{△}^{AlCl_{3}}$ +HCl.
+HCl.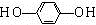 .
.