题目内容
2.下列说法正确的是( )| A. | 苯的同系物均可被酸性KMnO4溶液氧化 | |
| B. | 苯的同系物是分子中仅含有一个苯环的烃类物质 | |
| C. | 苯不能使酸性KMnO4溶液褪色,甲苯能使酸性KMnO4溶液褪色是因为甲苯中苯环对甲基的影响 | |
| D. | 相同质量的甲烷和乙烷完全燃烧甲烷耗氧量多 |
分析 A、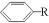 ,烷基R中直接与苯环连接的碳原子上没有C-H键,则不容易被氧化得到
,烷基R中直接与苯环连接的碳原子上没有C-H键,则不容易被氧化得到 ;
;
B、苯或苯的同系物必须满足通式CnH2n-6(n≥6),分子中只有一个苯环,且侧链为饱和链烃;
C、甲苯中苯环对甲基的影响,使甲基变得活泼能被KMnO4酸性溶液氧化;
D、相等质量的烃,H元素质量分数越大,耗氧量越大.
解答 解:A、烷基取代苯 可以被KMnO4的酸性溶液氧化生成
可以被KMnO4的酸性溶液氧化生成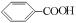 ,但若烷基R中直接与苯环连接的碳原子上没有C-H键,则不容易被氧化得到
,但若烷基R中直接与苯环连接的碳原子上没有C-H键,则不容易被氧化得到 ,故A错误;
,故A错误;
B、苯或苯的同系物,分子中只有一个苯环,且侧链必须不含不饱和键,若支链含有碳碳双键,则不是苯的同系物,如苯乙烯,故B错误;
C、苯不能使KMnO4酸性溶液褪色,甲苯中苯环对甲基的影响,使甲基的活性增强,能被KMnO4酸性溶液氧化,酸性KMnO4溶液褪色,故C正确;
D、相等质量的甲烷与乙烷,分子中C、H原子数目之比分别为1:4、1:3,故甲烷中H元素质量分数更大,则甲烷耗氧量更大,故D正确,故选CD.
点评 本题主要考查了有机物的性质,掌握基团的相互影响是解题的关键,难度不大.

练习册系列答案
相关题目
12.下列有关叙述错误的是( )
| A. | 纤维素和高级脂肪酸都是高分子化合物 | |
| B. | 天然油脂一般为多种混甘油酯的混合物,因此无固定的熔沸点 | |
| C. | 皂化反应完成后加入食盐可以使高级脂肪酸钠从混合物中析出,这一过程叫盐析 | |
| D. | 区别植物油和矿物油的正确方法是将它们分别加入氢氧化钠溶液,加热、振荡,观察是否分层 |
13.在一定体积的密闭容器中,进行如下反应:CO2(g)+H2(g)?CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
回答下列问题:
(1)该反应化学平衡常数的表达式:K=$\frac{c(CO)c({H}_{2}O)}{c(C{O}_{2})c({H}_{2})}$;
(2)该反应为吸热(填“吸热”或“放热”)反应;
(3)下列说法中能说明该反应达平衡状态的是B
A.容器中压强不变 B.混合气体中c(CO)不变
C.混合气体的密度不变 D.c(CO)=c(CO2)
E.单位时间内生成CO的分子数与生成H2O的分子数相等
(4)为了提高H2的转化率,下列措施可行的是D
A.降低温度 B.使用催化剂
C.增大压强 D.循环利用和不断补充CO2
(5)某温度下,各物质的平衡浓度符合下式:c(CO2)×c(H2)=c(CO)×c(H2O),试判此时的温度为830℃.
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应化学平衡常数的表达式:K=$\frac{c(CO)c({H}_{2}O)}{c(C{O}_{2})c({H}_{2})}$;
(2)该反应为吸热(填“吸热”或“放热”)反应;
(3)下列说法中能说明该反应达平衡状态的是B
A.容器中压强不变 B.混合气体中c(CO)不变
C.混合气体的密度不变 D.c(CO)=c(CO2)
E.单位时间内生成CO的分子数与生成H2O的分子数相等
(4)为了提高H2的转化率,下列措施可行的是D
A.降低温度 B.使用催化剂
C.增大压强 D.循环利用和不断补充CO2
(5)某温度下,各物质的平衡浓度符合下式:c(CO2)×c(H2)=c(CO)×c(H2O),试判此时的温度为830℃.
10.地壳中含量占第1、2位的元素间形成的化合物,不具有的性质是( )
| A. | 常温下与水反应生成酸 | B. | 高温时能与纯碱反应 | ||
| C. | 熔点高,硬度大 | D. | 常温下能与NaOH溶液反应 |
14.有关钢铁电化学腐蚀及保护的下列叙述中正确的是( )
| A. | 钢铁的电化学腐蚀过程可用原电池或电解池的原理来解释 | |
| B. | 可将河道中的钢铁闸门与外加直流电源的负极相连以保护其不受腐蚀 | |
| C. | 在钢铁表面镀锌属于牺牲阳极阴极保护法 | |
| D. | 钢铁的电化学腐蚀中,主要是吸氧腐蚀 |
11.韩国首尔大学的科学家将水置于一个足够强的电场中,在20℃时,水分子瞬间凝固形成“暖冰”.下列关于“暖冰”的说法正确的是( )
| A. | 暖冰中水分子是直线型分子 | |
| B. | 水凝固形成20℃时的“暖冰”所发生的变化是化学变化 | |
| C. | 暖冰中水分子是分子密堆积 | |
| D. | 在电场作用下,水分子间更易形成氢键,因而可以制得“暖冰” |
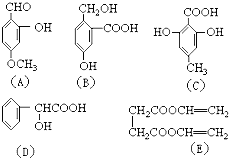 下列有机物中,有多个官能团:可以看作醇类的是
下列有机物中,有多个官能团:可以看作醇类的是