题目内容
3.下列说法错误的是( )| A. | 石油的裂化、油脂的硬化、煤的液化均属于化学变化 | |
| B. | 葡萄糖、蔗糖、麦芽糖均属于还原性糖 | |
| C. | 淀粉、纤维素均属于天然高分子化合物 | |
| D. | Al2O3、Al(OH)3、氨基酸均为两性化合物,能与酸、碱反应生成盐 |
分析 A、在反应过程中有新物质生成的属于化学变化;
B、蔗糖不含有醛基,不具有还原性;
C、相对分子质量大于10000的属于高分子化合物;
D、氧化铝、氢氧化铝和氨基酸均分别既能与酸反应又能与碱反应.
解答 解:A、煤的液化是利用煤制取甲醇,石油的裂化是将相对分子质量比较大的烃类断裂为相对分子质量较小的烃类来获得轻质油的过程,油脂的皂化是指油脂在碱性条件下的水解,均有新物质生成,均为化学变化,故A正确;
B、蔗糖不是还原性糖,故B错误;
C、淀粉、纤维素的相对分子质量均大于10000,且属于天然高分子化合物,故C正确;
D、氧化铝、氢氧化铝和氨基酸均分别既能与酸反应又能与碱反应,称为两性化合物,故D正确,故选B.
点评 本题主要考查的是糖类的性质、化学变化的定义、高分子化合物的概念,难度不大.

练习册系列答案
相关题目
13.下列各有机物的分类或命名正确的是( )
| A. | 对甲基苯酚( )属于芳香烃 )属于芳香烃 | B. |  TNT TNT | ||
| C. |  2-乙基丁烷 2-乙基丁烷 | D. | 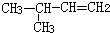 3-甲基-1-丁烯 3-甲基-1-丁烯 |
14.能在水溶液中大量共存的一组离子是( )
| A. | Fe3+、Mg2+、SCN-、Cl- | B. | Al3+、Mg2+、CO32-、Cl- | ||
| C. | K+、Ag+、Ca2+、NO3- | D. | Na+、H+、CH3COO-、Cl- |
11. 某同学按如图所示的装置(a、b是电极,c为电解质溶液)分别进行了下表列出的四组实验:
某同学按如图所示的装置(a、b是电极,c为电解质溶液)分别进行了下表列出的四组实验:
则有关叙述正确的是( )
 某同学按如图所示的装置(a、b是电极,c为电解质溶液)分别进行了下表列出的四组实验:
某同学按如图所示的装置(a、b是电极,c为电解质溶液)分别进行了下表列出的四组实验:| 组别 | a | b | c中的溶质 |
| 甲 | C | C | KOH |
| 乙 | Cu | Cu | NaCl |
| 丙 | Cu | Cu | CuSO4 |
| 丁 | C | C | NaCl |
| A. | 甲实验中溶液的pH要变小,两极均有气体放出 | |
| B. | 乙实验中发生反应的总反应式为:Cu+2H2O$\frac{\underline{\;通电\;}}{\;}$ Cu(OH)2↓+H2↑ | |
| C. | 丙实验中c溶液的浓度不变,a极质量增大 | |
| D. | 丁实验中a极电极反应式为:2H++2e-═H2↑ |
18.能用分液漏斗分离的混合物是( )
| A. | 液溴和四氯化碳 | B. | 乙醇和乙酸 | ||
| C. | 氯化钙和碳酸钠溶液 | D. | 苯和蒸馏水 |
15.下列关于海水资源综合利用的说法中,不正确的是( )
| A. | 从海水中富集镁元素可用Ca(OH)2沉淀法 | |
| B. | 海水淡化的方法主要有蒸馏法、离子交换法、电渗析法 | |
| C. | 从海水中提取溴单质的过程中用氯气做还原剂 | |
| D. | 从海水中获得粗盐可用蒸发结晶法 |
12.下列有关叙述错误的是( )
| A. | 纤维素和高级脂肪酸都是高分子化合物 | |
| B. | 天然油脂一般为多种混甘油酯的混合物,因此无固定的熔沸点 | |
| C. | 皂化反应完成后加入食盐可以使高级脂肪酸钠从混合物中析出,这一过程叫盐析 | |
| D. | 区别植物油和矿物油的正确方法是将它们分别加入氢氧化钠溶液,加热、振荡,观察是否分层 |
13.在一定体积的密闭容器中,进行如下反应:CO2(g)+H2(g)?CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表所示:
回答下列问题:
(1)该反应化学平衡常数的表达式:K=$\frac{c(CO)c({H}_{2}O)}{c(C{O}_{2})c({H}_{2})}$;
(2)该反应为吸热(填“吸热”或“放热”)反应;
(3)下列说法中能说明该反应达平衡状态的是B
A.容器中压强不变 B.混合气体中c(CO)不变
C.混合气体的密度不变 D.c(CO)=c(CO2)
E.单位时间内生成CO的分子数与生成H2O的分子数相等
(4)为了提高H2的转化率,下列措施可行的是D
A.降低温度 B.使用催化剂
C.增大压强 D.循环利用和不断补充CO2
(5)某温度下,各物质的平衡浓度符合下式:c(CO2)×c(H2)=c(CO)×c(H2O),试判此时的温度为830℃.
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应化学平衡常数的表达式:K=$\frac{c(CO)c({H}_{2}O)}{c(C{O}_{2})c({H}_{2})}$;
(2)该反应为吸热(填“吸热”或“放热”)反应;
(3)下列说法中能说明该反应达平衡状态的是B
A.容器中压强不变 B.混合气体中c(CO)不变
C.混合气体的密度不变 D.c(CO)=c(CO2)
E.单位时间内生成CO的分子数与生成H2O的分子数相等
(4)为了提高H2的转化率,下列措施可行的是D
A.降低温度 B.使用催化剂
C.增大压强 D.循环利用和不断补充CO2
(5)某温度下,各物质的平衡浓度符合下式:c(CO2)×c(H2)=c(CO)×c(H2O),试判此时的温度为830℃.
