题目内容
12.下列由相关实验现象所推出的结论正确的是( )| A. | Al与稀H2SO4、稀HNO3反应均生成铝盐并放出气体,说明Al与两种酸均发生置换反应 | |
| B. | 常温下浓硫酸能使铁和铝发生钝化,于是可在常温下用铁或铝制品贮藏、贮运浓硫酸 | |
| C. | Cl2和SO2均能使品红溶液褪色,说明二者都有氧化性 | |
| D. | 向溶液中滴加硝酸酸化的BaCl2溶液出现白色沉淀,说明该溶液中一定有SO42-或SO32-中的一种或两种 |
分析 A.铝与硝酸发生氧化还原反应生活NO和硝酸铝、水;
B.常温下浓硫酸能使铁和铝发生钝化,在表现生成致密的氧化物膜;
C.二氧化硫与有色有机物发生化合反应;
D.可能生成AgCl沉淀.
解答 解:A.Fe与稀HNO3反应生成NO,该反应不是置换反应,Fe与稀H2SO4反应有氢气生成,属于置换反应,故A错误;
B.常温下浓硫酸能使铁和铝发生钝化,在表现生成致密的氧化物膜,阻碍反应的继续进行,可在常温下用铁或铝制品贮藏、贮运浓硫酸,故B正确;
C.SO2与有色有机物发生化合反应,为非氧化还原反应,故C错误;
D.可能生成AgCl沉淀,应加入硝酸钡,故D错误.
故选B.
点评 本题考查较为综合,涉及元素化合物知识的综合理解和运用,有利于培养学生的良好科学素养和提高学习的积极性,难度不大,注意相关基础知识的积累和学习.

练习册系列答案
 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案
相关题目
20.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 1molCl2与足量的铁反应生成FeCl3,转移的电子数是3NA | |
| B. | 1mol氧气含有的原子数是1mol氖气含有的原子数的两倍 | |
| C. | 7.8g Na2O2中含有阴离子的数目为0.1NA,与足量水反应时电子转移了0.1NA | |
| D. | 在标准状况下,NA个水分子所占有的体积约为22.4L |
17.雾霾严重影响人们的生活与健康.某地区的雾霾中可能含有如下可溶性无机离子:Na+、NH4+、Mg2+、Al3+、SO42-、NO3-、Cl-.某同学收集了该地区的雾霾,经必要的预处理后试样溶液,设计并完成了如图的实验:
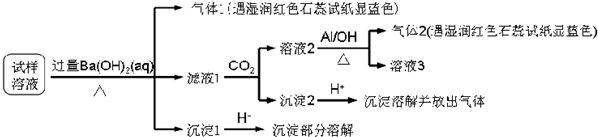
根据以上的实验操作与现象,该同学得出的结论不正确的是( )

根据以上的实验操作与现象,该同学得出的结论不正确的是( )
| A. | 试样中肯定存在NH4+、Mg2+、SO42-和NO3- | |
| B. | 试样中可能存在Na+、Cl- | |
| C. | 试样中一定不含Al3+ | |
| D. | 该雾霾中可能存在NaNO3、NH4Cl和MgSO4 |
4.下列指定反应的离子方程式正确的是( )
| A. | 氯气溶于水:Cl2+H2O?2H++Cl-+ClO- | |
| B. | Na2CO3溶液中加入少量稀盐酸:CO32-+2H+═CO2↑+H2O | |
| C. | 酸性溶液中KIO3与KI反应生成I2:IO3-+I-+6H+═I2+3H2O | |
| D. | NaHCO3溶液中加足量Ba(OH)2溶液:HCO3-+Ba2++OH-═BaCO3↓+H2O |
2.H2O2(l)在有MnO2条件下和无MnO2条件下分解的能量变化如图所示,下列说法正确的是( )

| A. | 有MnO2条件下的反应曲线是a曲线 | |
| B. | a曲线变为b曲线,反应的活化分子百分数增大 | |
| C. | a曲线变为b曲线,平衡时H2O2的转化率增大 | |
| D. | b曲线的热化学方程式为:H2O2(l)═H2O(l)+$\frac{1}{2}$O2(g)△H=-(E1-E2)KJ•mol-1 |
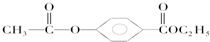 .A经①②两步反应得到C、D和E.B经①②两步反应得E、F和H.上述反应过程、产物性质及相互关系如图所示.
.A经①②两步反应得到C、D和E.B经①②两步反应得E、F和H.上述反应过程、产物性质及相互关系如图所示.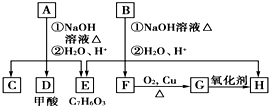
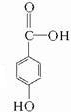 .
.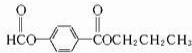 和
和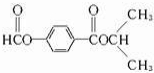 .
.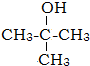 .
.