题目内容
下列有关说法正确的是( )
| A、单质Na可通过电解NaCl溶液制得 |
| B、石灰乳与Cl2的反应中,Cl2既是氧化剂,又是还原剂 |
| C、常温下干燥的Cl2能用钢瓶贮存,所以Cl2不与铁反应 |
| D、25℃,NaHCO3在水中的溶解度比Na2CO3的大 |
考点:钠的化学性质,氯气的化学性质,钠的重要化合物
专题:元素及其化合物
分析:A.制钠是电解熔融NaCl来制取,电解NaCl溶液制得氯气和氢氧化钠和氢气;
B.从元素化合价的变化的角度分析,氧化还原反应中,氧化剂得到电子被还原,所含元素的化合价降低,还原剂失去电子被氧化,所含元素的化合价升高;
C.常温下干燥的Cl2能用钢瓶贮存,但Cl2能与铁反应,铁在氯气中燃烧生成氯化铁;
D.25℃,Na2CO3的溶解度比NaHCO3大;
B.从元素化合价的变化的角度分析,氧化还原反应中,氧化剂得到电子被还原,所含元素的化合价降低,还原剂失去电子被氧化,所含元素的化合价升高;
C.常温下干燥的Cl2能用钢瓶贮存,但Cl2能与铁反应,铁在氯气中燃烧生成氯化铁;
D.25℃,Na2CO3的溶解度比NaHCO3大;
解答:
解:A.电解纯净的NaCl溶液:2NaCl+2H2O
2NaOH+H2↑+Cl2↑,得不到钠,工业制钠是电解熔融NaCl:2NaCl
2Na+Cl2↑,故A错误;
B.石灰乳与Cl2的反应2Cl2+2Ca(OH)2═Ca(ClO)2+CaCl2+2H2O,氯元素的化合价从Cl2单质0价,变为生成物次氯酸钙中的+1价,是还原剂,变为氯化钙中-1价的氯,是氧化剂,所以该反应中Cl2既是氧化剂,又是还原剂,故B正确;
C.潮湿的氯气易与钢瓶反应,为防止氯气腐蚀钢瓶,钢瓶在装入氯气前必须干燥,铁在氯气中燃烧生成氯化铁,方程式为2Fe+3Cl2
2FeCl3,故C错误;
D.在相同温度下,Na2CO3较NaHCO3溶解度大,可通过在饱和碳酸钠溶液中通入过量二氧化碳溶液变浑浊验证,故D错误;
故选B.
| ||
| ||
B.石灰乳与Cl2的反应2Cl2+2Ca(OH)2═Ca(ClO)2+CaCl2+2H2O,氯元素的化合价从Cl2单质0价,变为生成物次氯酸钙中的+1价,是还原剂,变为氯化钙中-1价的氯,是氧化剂,所以该反应中Cl2既是氧化剂,又是还原剂,故B正确;
C.潮湿的氯气易与钢瓶反应,为防止氯气腐蚀钢瓶,钢瓶在装入氯气前必须干燥,铁在氯气中燃烧生成氯化铁,方程式为2Fe+3Cl2
| ||
D.在相同温度下,Na2CO3较NaHCO3溶解度大,可通过在饱和碳酸钠溶液中通入过量二氧化碳溶液变浑浊验证,故D错误;
故选B.
点评:本题考查氯、钠的性质,侧重于基础知识的考查,涉及氯碱工业原理、氯气贮存、Na2CO3与NaHCO3溶解度比较等知识点,有利于培养学生的良好的科学素养,注意通过在饱和碳酸钠溶液中通入过量二氧化碳溶液变浑浊验证Na2CO3的溶解度比NaHCO3大,题目难度不大.

练习册系列答案
相关题目
反应3H2(g)+N2(g)?2NH3(g)△H=-46.19kJ?mol-1,关于这个反应的平衡常数K,下列说法正确的是( )
| A、随温度升高K增加 |
| B、随压强升高K增加 |
| C、随温度升高K减小 |
| D、随压强升高K减小 |
下列离子方程式正确的是( )
| A、小苏打溶液中加入醋酸:HCO3-+H+═CO2↑+H2O |
| B、碳酸氢铵溶液和足量氢氧化钠溶液混合:NH4++OH-═NH3?H2O |
| C、NaHS水解:HS-+H2O═S2-+H3O+ |
| D、硫酸亚铁溶液中滴加酸化的双氧水:2Fe2++2H++H2O2═2Fe3++2H2O |
下列反应中,生成的有机物只有一种的是( )
A、异戊二烯(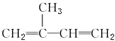 )与等物质的量的Br2发生加成反应 )与等物质的量的Br2发生加成反应 |
| B、2氯丁烷与NaOH乙醇溶液共热发生消去HCl分子的反应 |
| C、新戊烷和氯气发生取代反应生成一氯取代物 |
| D、甲苯在一定条件下发生硝化反应生成一硝基甲苯 |
下列说法不正确的是( )
| A、长期使用阿司匹林会出现水杨酸中毒表现,应立即停药,静脉注射碳酸氢钠溶液 |
| B、红宝石、水晶、钻石的主要成分都是硅酸盐 |
| C、高温条件下可杀死H7N9型禽流感病毒,属于蛋白质的变性 |
| D、石油裂解、煤的气化、海水制镁都包含化学变化 |
分别将下列物质:①FeCl3②Na2O2③NaCl④Ca(HCO3)2投入水中,对其溶液加热蒸干,仍能得到原物质的是( )
| A、①②③ | B、①③ | C、③④ | D、③ |
下列混合溶液中,各离子浓度的大小关系不正确的是( )
| A、物质的量浓度相等CH3COOH和CH3COONa溶液等体积混合:c(CH3COO-)+c(CH3COOH)=2c(Na+) |
| B、0.1mol/L Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+c(H2CO3) |
| C、物质的量浓度相等Na2CO3和NaHCO3溶液等体积混合,离子浓度的大小顺序是:c (Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+) |
| D、NH4Cl溶液中:c(H+)=c(NH3?H2O)+c(OH-) |
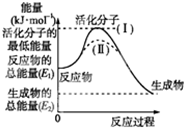 请认真观察图,然后回答问题.
请认真观察图,然后回答问题.