题目内容
【题目】常温向20mL 0.1mol·L-1氨水中滴加0.1mol·L-1盐酸,溶液pH随滴加盐酸溶液体积的变化如图2所示。下列说法正确的是
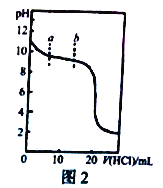
A. a点时,c(NH3·H2O)>c(C1-)>c(NH4+)>c(OH-)>c(H+)
B. a~b区域内c(NH4+)+c(NH3·H2O)=0.1mol·L-1
C. 当V(HC1)=10mL时,c(NH4+)-c(NH3·H2O)=2[c(OH-)-c(H+)]
D. 当V(HCl)=20mL时,c(H+)+c(C1-)>c(NH4+)+c(NH3·H2O)+c(OH-)
【答案】CD
【解析】A项,滴入盐酸后溶液中的电荷守恒为:c(NH4+)+c(H+)=c(Cl-)+c(OH-),违背电荷守恒,错误;B项,根据物料守恒,c(NH4+)+c(NH3·H2O)=![]() ,a~b区域,V(HCl)
,a~b区域,V(HCl)![]() 0,则c(NH4+)+c(NH3·H2O)
0,则c(NH4+)+c(NH3·H2O)![]() 0.1mol/L,错误;C项,当V(HCl)=10mL,盐酸与氨水反应后得等物质的量浓度的NH4Cl和氨水的混合液,溶液中电荷守恒为:c(NH4+)+c(H+)=c(Cl-)+c(OH-),物料守恒为:c(NH4+)+c(NH3·H2O)=2c(Cl-),两式整理得,c(NH4+)- c(NH3·H2O)=2[c(OH-)- c(H+)],正确;D项,当V(HCl)=20mL,盐酸与氨水恰好完全反应得0.05mol/L的NH4Cl溶液,由于NH4+的水解溶液呈酸性,溶液中c(H+)
0.1mol/L,错误;C项,当V(HCl)=10mL,盐酸与氨水反应后得等物质的量浓度的NH4Cl和氨水的混合液,溶液中电荷守恒为:c(NH4+)+c(H+)=c(Cl-)+c(OH-),物料守恒为:c(NH4+)+c(NH3·H2O)=2c(Cl-),两式整理得,c(NH4+)- c(NH3·H2O)=2[c(OH-)- c(H+)],正确;D项,当V(HCl)=20mL,盐酸与氨水恰好完全反应得0.05mol/L的NH4Cl溶液,由于NH4+的水解溶液呈酸性,溶液中c(H+)![]() c(OH-),溶液中的物料守恒为c(NH4+)+c(NH3·H2O)=c(Cl-),则c(H+)+ c(Cl-)> c(NH4+)+c(NH3·H2O)+ c(OH-),正确;答案选CD。
c(OH-),溶液中的物料守恒为c(NH4+)+c(NH3·H2O)=c(Cl-),则c(H+)+ c(Cl-)> c(NH4+)+c(NH3·H2O)+ c(OH-),正确;答案选CD。

 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案【题目】下列化学实验事实及其结论都正确的是
选项 | 实验事实 | 结论 |
A | 向装有Fe(NO3)2溶液的试管中加入稀H2SO4,在管口观察到红棕色气体, | HNO3分解成了NO2 |
B | 向某溶液中加入2滴KSCN溶液,溶液不显红色。再向溶液中加入几滴新制的氯水,溶液变为红色 | 该溶液中一定含有Fe2+ |
C | 取久置的Na2O2粉末,向其中滴加过量的盐酸,产生无色气体 | Na2O2没有变质 |
D | 取某溶液少量,加入盐酸酸化的氯化钡溶液,出现白色沉淀 | 该溶液中一定含有大量的SO |
A. A B. B C. C D. D
【题目】硫酸镁晶体(MgSO4·7H2O)是一种重要的化工原料。以菱镁矿(主要成分是MgCO3,含少量FeCO3和不溶性杂质)为原料制取硫酸镁晶体的流程如下:
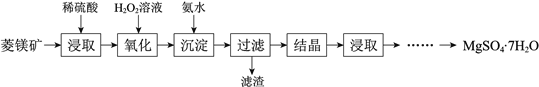
(1)MgCO3溶于稀硫酸的离子方程式是_________________________。
(2)加入H2O2溶液的目的是____________________(用离子方程式表示)。
(3)已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
阳离子 | Mg2+ | Fe2+ | Fe3+ |
开始沉淀 | 9.1 | 7.6 | 1.9 |
完全沉淀 | 11.1 | 9.7 | 3.2 |
“沉淀”步骤中,用氨水调节溶液pH的范围是______________________________。
(4)“过滤”所得滤液中存在大量的阳离子有Mg2+、____________。
(5)“结晶”步骤中需蒸发浓缩滤液,使用的仪器有铁架台、酒精灯和_________________。




