题目内容
20.有下列几组物质或微粒:(1)属于同分异构体的是D;
(2)属于同位素的是A;
(3)属于同一种物质的是E;
(4)属于同系物的是B.
A.11H和12H B.甲烷和乙烷 C.金刚石、石墨和C60 D.丁烷和异丁烷
E.
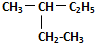 和
和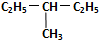 .
.
分析 (1)同分异构体是具有相同的分子式和不同结构的有机物之间的互称;
(2)质子数相同,中子数不同的原子互称同位素;
(3)结构、分子式一样的属于同种物质;
(4)结构相似,分子组成上相差1个或者若干个CH2基团的化合物互称为同系物.
解答 解:A.11H和12H,质子数相同,中子数不同,属于同位素;
B.甲烷和乙烷,结构相似,分子组成上相差1个CH2基团,属于同系物;
C.金刚石、石墨和C60,均是碳元素形成的不同种单质,互为同素异形体;
D.丁烷和异丁烷,分子式相同,结构不同,属于同分异构体;
E. 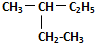 和
和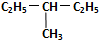 ,分子式相同,结构相同,属于同种物质,
,分子式相同,结构相同,属于同种物质,
故答案为:(1)D;(2)A;(3)E;(4)B.
点评 本题考查了同分异构体、同位素、同素异形体、同系物的判断,题目难度不大,明确概念是解本题的关键.

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目
11. 某课外兴趣小组对H2O2的分解速率做了如下实验探究.
某课外兴趣小组对H2O2的分解速率做了如下实验探究.
(1)下表是该小组研究影响过氧化氢(H2O2)分解速率的因素时采集的一组数据:用10mL H2O2制取150mLO2所需的时间(秒)
①该小组在设计方案时,考虑了浓度、a:温度、b:催化剂等因素对过氧化氢分解速率的影响.
②从上述影响H2O2分解速率的因素a和b中任选一个,说明该因素对该反应速率的影响:其他条件不变,升高反应温度,H2O2分解速率加快.
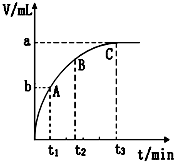
(2)某同学在10mL H2O2 溶液中加入一定量的二氧化锰,放出气体的体积(标准状况)与反应时间的关系如如图所示,
①写出H2O2发生的化学反应方程式2H2O2$\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2↑.
②A、B、C三点所表示的即时反应速率最慢的是C.
(3)若将适量MnO2加入酸化的H2O2的溶液中,MnO2溶解产生Mn2+,另外,产物中还有O2产生,请写出该反应的离子方程式MnO2+2H++H2O2=Mn2++O2↑+2H2O.
 某课外兴趣小组对H2O2的分解速率做了如下实验探究.
某课外兴趣小组对H2O2的分解速率做了如下实验探究.(1)下表是该小组研究影响过氧化氢(H2O2)分解速率的因素时采集的一组数据:用10mL H2O2制取150mLO2所需的时间(秒)
| 30%H2O2 | 15%H2O2 | 10%H2O2 | 5%H2O2 | |
| 无催化剂、不加热 | 几乎不反应 | 几乎不反应 | 几乎不反应 | 几乎不反应 |
| 无催化剂、加热 | 360 | 480 | 540 | 720 |
| MnO2催化剂、加热 | 10 | 25 | 60 | 120 |
②从上述影响H2O2分解速率的因素a和b中任选一个,说明该因素对该反应速率的影响:其他条件不变,升高反应温度,H2O2分解速率加快.
(2)某同学在10mL H2O2 溶液中加入一定量的二氧化锰,放出气体的体积(标准状况)与反应时间的关系如如图所示,
①写出H2O2发生的化学反应方程式2H2O2$\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2↑.
②A、B、C三点所表示的即时反应速率最慢的是C.
(3)若将适量MnO2加入酸化的H2O2的溶液中,MnO2溶解产生Mn2+,另外,产物中还有O2产生,请写出该反应的离子方程式MnO2+2H++H2O2=Mn2++O2↑+2H2O.
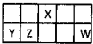
8. Ⅰ.短周期元素X、Y、Z、W在元素周期表中相对位置如图所示,其中Y所处的周期序数与族序数相等.按要求回答下列问题:
Ⅰ.短周期元素X、Y、Z、W在元素周期表中相对位置如图所示,其中Y所处的周期序数与族序数相等.按要求回答下列问题:
(1)写出X的原子结构示意图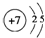 .
.
(2)Y、Z、W的简单离子半径由大到小顺序为S2->Cl->Al3+(用离子符号表示).
(3)含Y的某种盐常用作净水剂,其净水原理是Al3+3H2O?Al(OH)3(胶体)+3H+(用离子方程式表示).
Ⅱ.运用所学化学原理,解决下列问题:
(4)已知:①C(s)+O2(g)═CO2(g);△H=a kJ•mol-1;
②CO2(g)+C(s)═2CO(g);△H=b kJ•mol-1;
③Si(s)+O2(g)═SiO2(s);△H=c kJ•mol-1.
工业上生产粗硅的热化学方程式为2C(s)+SiO2(s)=2CO(g)+Si(s)△H=(a+b-c)kJ•mol-1.
(5)已知:CO(g)+H2O(g)?H2(g)+CO2(g).表为该反应在不同温度时的平衡常数.该反应的△H<0(填“>”、“<”);500℃时进行该反应,且CO和H2O起始浓度相等,CO平衡转化率为75%.
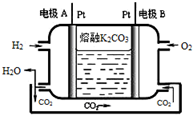
(6)以熔融K2CO3为电解质的一种新型氢氧燃料电池工作原理如图所示.写出电极A的电极反应式H2-2e-+CO32-═CO2+H2O.
 Ⅰ.短周期元素X、Y、Z、W在元素周期表中相对位置如图所示,其中Y所处的周期序数与族序数相等.按要求回答下列问题:
Ⅰ.短周期元素X、Y、Z、W在元素周期表中相对位置如图所示,其中Y所处的周期序数与族序数相等.按要求回答下列问题:
(1)写出X的原子结构示意图
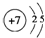 .
.(2)Y、Z、W的简单离子半径由大到小顺序为S2->Cl->Al3+(用离子符号表示).
(3)含Y的某种盐常用作净水剂,其净水原理是Al3+3H2O?Al(OH)3(胶体)+3H+(用离子方程式表示).
Ⅱ.运用所学化学原理,解决下列问题:
(4)已知:①C(s)+O2(g)═CO2(g);△H=a kJ•mol-1;
②CO2(g)+C(s)═2CO(g);△H=b kJ•mol-1;
③Si(s)+O2(g)═SiO2(s);△H=c kJ•mol-1.
工业上生产粗硅的热化学方程式为2C(s)+SiO2(s)=2CO(g)+Si(s)△H=(a+b-c)kJ•mol-1.
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
(6)以熔融K2CO3为电解质的一种新型氢氧燃料电池工作原理如图所示.写出电极A的电极反应式H2-2e-+CO32-═CO2+H2O.
12.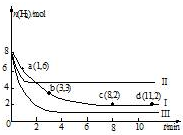 一定温度下,向容积为2L的恒容密闭容器中充入6molCO2和8molH2,发生反应:
一定温度下,向容积为2L的恒容密闭容器中充入6molCO2和8molH2,发生反应:
CO2(g)+3H2?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1,测得n(H2)随时间变化如曲线I所示.下列说法正确的是( )
 一定温度下,向容积为2L的恒容密闭容器中充入6molCO2和8molH2,发生反应:
一定温度下,向容积为2L的恒容密闭容器中充入6molCO2和8molH2,发生反应:CO2(g)+3H2?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1,测得n(H2)随时间变化如曲线I所示.下列说法正确的是( )
| A. | 该反应在0~8min内CO2的平均反应速率是0.375mol•L-1•min-1 | |
| B. | 若起始时向上述容器中充入3molCO2和4molH2,则平衡时H2的条件分数大于20% | |
| C. | 若起始是向上述容器中充入4molCO2、2molH2、2molCH3OH和1molH2O(g),则此是反应向正反应方向进行 | |
| D. | 改变条件得到曲线II、III,则曲线II、III改变的他分别是升高温度、充入氢气 |
9.下列关于常见物质的工业冶炼说法正确的是( )
| A. | 工业制金属钠:电解饱和食盐水 | |
| B. | 工业制溴:某些植物有富集溴的能力,从海产品中提取溴是工业上获取溴的重要途径 | |
| C. | 冶炼铝:电解Al2O3,同时加入冰晶石(Na3AlF6),目的是为了降低Al2O3熔融温度 | |
| D. | 硫酸工业:在氧气充足的情况下,从接触室进入吸收塔的气体中不可能含有SO2 |
10.下列装置或操作能达到目的是( )
| A. | 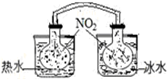 依据两容器内气体颜色变化,判断反应2NO2(g)?N2O4(g)平衡移动的方向 | |
| B. | 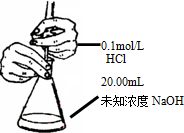 测定锥形瓶内的NaOH的浓度 | |
| C. | 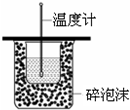 测定中和热 | |
| D. | 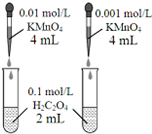 依据褪色快慢比较浓度对反应速率的影响 |
 .实验室制取并检验气体A的方法是2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O,将湿润的红色石蕊试纸靠近气体,若试纸变蓝,则是氨气.
.实验室制取并检验气体A的方法是2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O,将湿润的红色石蕊试纸靠近气体,若试纸变蓝,则是氨气.