��Ŀ����
����Ŀ������Ȳ����ۺ���ĺϳ�ʹ�߷��Ӳ��Ͻ��������ϳɽ����������ϵ���ѧʱ�������� ��Ȳ���Ӵ���ҩ�������ȷ���Ƭ�κ;�����һ����������ԡ��������ҹ���ѧ�� �������ϳɵľ���Ȳ��������� M �Ľṹʽ�� M ��ϡ���������µ�ˮ����̡�
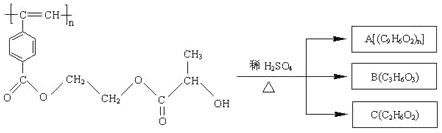
�����й�˵��������ȷ����
A. M �� A ����ʹ���Ը��������Һ����ˮ��ɫ
B. B �к������ֹ����ţ�B �ܷ�����ȥ��Ӧ�����۷�Ӧ
C. A��B��C �� 1 mol �ֱ����������Ʒ�Ӧ���ų�����������ʵ���֮��Ϊ 1��2��2
D. 1 mol M ���ȵ��ռ���Һ��Ӧ�������� 2n mol �� NaOH
���𰸡�C
��������
Mˮ������A�Ľṹ��ʽ��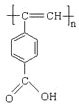 ��B��CH3CH��OH��COOH��C��HOCH2CH2OH���������������������ŷ�������
��B��CH3CH��OH��COOH��C��HOCH2CH2OH���������������������ŷ�������
A. M�� A������̼̼˫�������Ծ���ʹ���Ը��������Һ����ˮ��ɫ����A��ȷ��
B. B��CH3CH��OH��COOH���������ֹ����ţ��ǻ��������ǻ�ֱ������̼ԭ�ӵ���̼����Hԭ�ӣ����Ȼ�������B �ܷ�����ȥ��Ӧ�����۷�Ӧ����B��ȷ��
C. A��B��C �� 1 mol �ֱ������������Ʒ�Ӧ���ų�����������ʵ���֮��Ϊ n��2��2����C����
D. 1 mol M �к���2n mol����������1 mol M���ȵ��ռ���Һ��Ӧ�������� 2n mol �� NaOH����D��ȷ��

 ����������������ϵ�д�
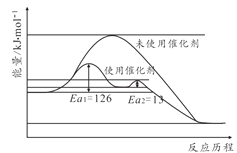
����������������ϵ�д�����Ŀ���ϳɰ������������ͷ�չ������Ҫ���壬1909�������ʵ�������״����õ�����������Ӧ�ϳɰ���ʵ�����˹��̵���
��1����ӦN2(g) + 3H2(g) ![]() 2NH3(g)�Ļ�ѧƽ�ⳣ������ʽΪ______��
2NH3(g)�Ļ�ѧƽ�ⳣ������ʽΪ______��
��2�������������ݷ�������ҵ��ѡ�õ�����������Ӧ�̵�����û��ѡ�õ�����������
Ӧ�̵���ԭ����______��
��� | ��ѧ��Ӧ | K(298K)����ֵ |
�� | N2(g) + O2(g) | 5��10-31 |
�� | N2(g) + 3H2(g) | 4.1��106 |
��3�����ڷ�ӦN2(g)+3H2(g)![]() 2NH3(g)����һ�������°���ƽ�⺬�����±���
2NH3(g)����һ�������°���ƽ�⺬�����±���
�¶�/�� | ѹǿ/MPa | ����ƽ�⺬�� |
200 | 10 | 81.5% |
550 | 10 | 8.25% |
�� �÷�ӦΪ______������ȡ����ȡ�����Ӧ��
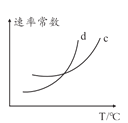
�� ������������ʱ���¶����߰���ƽ�⺬����С��ԭ����______������ĸ��ţ���
a. �¶����ߣ�����Ӧ���ʼ�С���淴Ӧ��������ƽ�������ƶ�
b. �¶����ߣ�Ũ����(Q)���Q > K��ƽ�������ƶ�
c. �¶����ߣ�����������࣬��Ӧ���ʼӿ�
d. �¶����ߣ�K��С��ƽ�������ƶ�
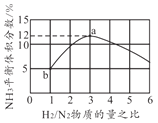
�� ����ѡ�õ�������550�桢10 MPa������200�桢10 MPa�����ܵ�ԭ����______��
��4��һ���¶��£����ݻ��㶨���ܱ������г���1 mol ������3 mol������һ��ʱ���ﻯѧƽ��״̬�������������������䣬������ƽ����ϵ���ٳ���1 mol������3 mol ������������ƽ��ת����______��������С�����䡱����
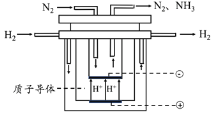
��5�����ܹ����ĺϳɰ�������Ϊ��20���Ϳ�ѧ��������Ի͵ijɾ͡�֮һ�����Դ��ں��ܸߡ����ʵ͵����⡣��ˣ���ѧ���ڳ���̽����Ѱ��ϳɰ�����·������ͼΪ��ⷨ�ϳɰ���ԭ��ʾ��ͼ�������ĵ缫��ӦʽΪ______��
����Ŀ������ʵ����Ҫ�������Լ���ѡ���ܴﵽʵ��Ŀ�ĵ���
ѡ�� | ��Ҫ���� | �Լ� | ʵ��Ŀ�� |
A | ��ƿ������©�����ƾ��ơ����� | ���̿���Ũ���� | ��ȡ���ռ���������� |
B | �ƾ��ơ������������������ż� |
| ������Һ�õ����� |
C | Բ����ƿ�������ܡ��ձ�������̨ | ����İ�����ˮ | ģ����Ȫʵ�� |
D | ��˿����ɫ�ܲ������ƾ��� | ���ᡢ����Һ | ��ɫ��Ӧʵ�� |
A.AB.BC.CD.D