题目内容
【题目】如图所示(B中冷却装置未画出),将氯气和空气(不参与反应)以体积比约1∶3混合通入含水8%的碳酸钠中制备Cl2O,并用水吸收Cl2O制备次氯酸溶液。
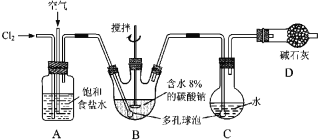
已知:Cl2O极易溶于水并与水反应生成HClO;Cl2O的沸点为3.8 ℃,42 ℃以上分解为Cl2和O2。
(1)①实验中控制氯气与空气体积比的方法是________________________________。
②为使反应充分进行,实验中采取的措施有______________________________。
③装置D的作用是____________________________________。
(2)①装置B中产生Cl2O的化学方程式为:____________________________________。
②若B无冷却装置,则进入C中的Cl2O会大量减少。其原因是_____________________。
(3)装置C中采用棕色圆底烧瓶是因为______________________________________。
(4)已知次氯酸可被H2O2、FeCl2等物质还原成Cl-。测定C中次氯酸溶液的物质的量浓度的实验方案为:用_____取20.00 mL次氯酸溶液,加入足量的_________________,再加入足量的_______________,过滤,洗涤沉淀,在真空干燥箱中干燥,用电子天平称量沉淀质量。 (可选用的试剂:H2O2溶液、FeCl2溶液、AgNO3溶液)。
【答案】通过观察A中产生气泡的速率调节流速 搅拌、使用多孔球泡 吸收未反应的氯气,防止污染空气 2Cl2+Na2CO3===Cl2O+2NaCl+CO2 该反应放热,温度升高Cl2O会分解 HClO见光易分解 酸式滴定管 H2O2溶液 硝酸银溶液
【解析】
氯气通过A装置与空气形成1:3的混合气体通入B装置,在搅拌棒的作用下与含水8%的碳酸钠充分反应制备Cl2O,并用水吸收Cl2O制备次氯酸钠溶液,同时用碱石灰吸收含有Cl2O的尾气,防止污染环境,(1)①控制氯气与空气体积比的方法可以通过观察A中产生气泡的比例来调节气体的流速;②增加气体与溶液的接触面积、搅拌等措施都可以加快反应速率;③装置D的作用是是吸收未反应的氯气,防止污染空气;(2)①装置B中,氯气本身既作为氧化剂又作还原剂,本身被氧化到+1价的Cl2O,被还原到-1价的氯化钠;②由于该反应为放热反应,温度升高Cl2O会分解,故进入C中的Cl2O会大量减少;(3)装置C是用水吸收Cl2O制备次氯酸溶液,但生成的HClO见光易分解,反应装置须选择避光;(4)需要20.00mL的次氯酸溶液,根据精确度应选用酸、碱式滴管,再根据HClO溶液既有酸性,又有强氧化性确定滴定管的类型;实验原理是结合所提供的试剂H2O2是还原HClO生成Cl-,再滴加过量提供的硝酸银溶液,根据生成的AgCl沉淀质量计算原溶液HClO的浓度。
(1)①通过观察A中产生气泡的速率调节气体的流速可以控制氯气与空气体积比的方法;②多孔球泡增加气体与溶液的接触面积可以加快反应速率;为使反应充分进行,实验中采取的措施有搅拌、使用多孔球泡;③装置D的作用是吸收未反应的氯气,防止污染空气;
(2)①装置B中,氯氯气和碳酸钠反应生成Cl2O,化学方程式为:2Cl2+Na2CO3=Cl2O+2NaCl+CO2;②由于该反应为放热反应,温度升高Cl2O会分解,故进入C中的Cl2O会大量减少;
(3)水吸收Cl2O制备次氯酸溶液,HClO见光易分解,故装置C中采用棕色圆底烧瓶;
(4)次氯酸溶液既有酸性,又有强氧化性,应选用酸式滴定管;具体实验操作是,向20.00mL的次氯酸溶液里加入足量的H2O2溶液,再加入足量的AgNO3溶液,过滤、洗涤,在真空干燥箱中干燥沉淀,用电子天平称量沉淀的质量。

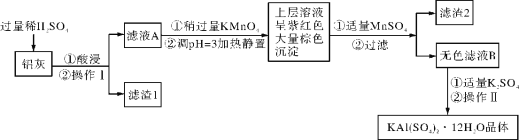
【题目】草酸铁晶体Fe2(C2O4)3·xH2O可溶于水,且能做净水剂。为测定该晶体中铁的含量,做了如下实验:
步骤1:称量5.6g草酸铁晶体,配制成250 mL一定物质的量浓度的溶液。
步骤2:取所配溶液25.00 mL于锥形瓶中,先加足量稀H2SO4酸化,再滴加KMnO4溶液,反应为:2KMnO4+5H2C2O4+3H2SO4═ K2SO4+2MnSO4+10CO2↑+8H2O。向反应后的溶液加锌粉,加热至黄色刚好消失,过滤、洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时溶液仍呈酸性。
步骤3:用0.0200 mol/LKMnO4溶液滴定步骤2所得溶液至终点,消耗KMnO4溶液V1 mL,滴定中MnO4-被还原成Mn2+。
重复步骤2、步骤3的操作2次,分别滴定消耗0.0200 mol/LKMnO4溶液为V2、V3 mL。
记录数据如下表:
实验编号 | KMnO4溶液的浓度(mol/L) | KMnO4溶液滴入的体积(mL) |
1 | 0.0200 | V1 = 20.02 |
2 | 0.0200 | V3 = 19.98 |
3 | 0.0200 | V2 = 23.32 |
请回答下列问题:
(1)草酸铁溶液能做净水剂的原因______________________________(用离子方程式表示)。
(2)步骤2加入酸性高锰酸钾的作用_________________________________________________。
(3)加入锌粉的目的是______________________________。
(4)步骤3滴定时滴定终点的判断方法是_____________________________________________。
(5)在步骤3中,下列滴定操作使测得的铁含量偏高的有______。
A.滴定管用水洗净后直接注入KMnO4溶液
B.滴定管尖嘴内在滴定前有气泡,滴定后气泡消失
C.读取KMnO4溶液体积时,滴定前平视,滴定结束后仰视读数
D.锥形瓶在滴定时剧烈摇动,有少量液体溅出.
(6)实验测得该晶体中铁的含量为_________。