题目内容
1.工业上利用硅的氧化物制取硅单质,主要反应为:SiO2+2C$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑.该反应中,还原剂是C(填化学式),被还原的物质是SiO2(填化学式);若反应中消耗了2mol C,则生成1mol Si,转移电子的物质的量为4mol.分析 反应SiO2+2C $\frac{\underline{\;高温\;}}{\;}$Si+2CO中,Si元素化合价降低,被还原,SiO2为氧化剂,C元素化合价升高,被氧化,C为还原剂,结合反应的化学方程式解答该题.
解答 解:反应SiO2+2C $\frac{\underline{\;高温\;}}{\;}$Si+2CO中Si元素化合价降低,被还原,SiO2为氧化剂,C元素化合价升高,被氧化,C为还原剂,由方程式可知,若反应中消耗了2mol C,则生成1mol Si,转移电子的物质的量为(2-0)×2mol=4mol.
故答案为:C;SiO2;1;4.
点评 本题考查氧化还原反应,为高考高频考点,侧重于化学与工业生产的考查,有利于培养学生的良好的科学素养,提高学习的积极性,注意从元素化合价的角度解答该题,难度不大.

练习册系列答案
相关题目
12. 下表各组物质之间通过一步反应不能实现如图所示转化的是( )
下表各组物质之间通过一步反应不能实现如图所示转化的是( )
 下表各组物质之间通过一步反应不能实现如图所示转化的是( )
下表各组物质之间通过一步反应不能实现如图所示转化的是( )| 选项 | X | Y | Z |
| A | SO2 | SO3 | H2SO4 |
| B | NaOH | Na2CO3 | Na2SO4 |
| C | Si | SiO2 | H2SiO3 |
| D | NO | NO2 | HNO3 |
| A. | A | B. | B | C. | C | D. | D |
9.下列实验现象与氧化还原反应有关的是( )
| A. | NH3使湿润的红色石蕊试纸变蓝 | |
| B. | NO气体遇空气由无色变为红棕色 | |
| C. | 向硅酸钠溶液中滴加适量的稀盐酸,有透明的凝胶形成 | |
| D. | 向Fe2(SO4)3溶液中滴加NaOH溶液,生成红褐色沉淀 |
6.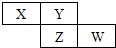 X,Y,Z,W均为短周期元素,它们在元素周期表中的位置如图所示.若Y原子的最外层电子数是次外层电子数的3倍,下列说法不正确的是( )
X,Y,Z,W均为短周期元素,它们在元素周期表中的位置如图所示.若Y原子的最外层电子数是次外层电子数的3倍,下列说法不正确的是( )
 X,Y,Z,W均为短周期元素,它们在元素周期表中的位置如图所示.若Y原子的最外层电子数是次外层电子数的3倍,下列说法不正确的是( )
X,Y,Z,W均为短周期元素,它们在元素周期表中的位置如图所示.若Y原子的最外层电子数是次外层电子数的3倍,下列说法不正确的是( )| A. | Y的氢化物在常温下为液态 | |
| B. | 最高价氧化物对应水化物的酸性:W>Z | |
| C. | 最低价氢化物稳定性:Y>X | |
| D. | 原子半径:W>Z>Y>X |
6.可以将六种无色液体:C2H5OH、C6H6、AgNO3溶液,NaOH溶液、KI溶液、C6H5OH溶液,区分开的试剂是( )
| A. | 碘水 | B. | 淀粉溶液 | C. | FeCl3溶液 | D. | 新制氢氧化铜 |
3.己烷的同分异构体除正己烷、2-甲基戊烷、2,2-二甲基丁烷、2,3-二甲基丁烷外,还有下列中的( )
| A. | 2-乙基丁烷 | B. | 2-甲基丁烷 | C. | 3-甲基戊烷 | D. | 2,2-甲基戊烷 |
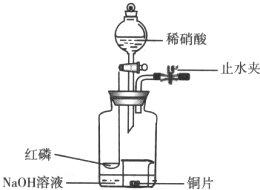 用如图示装置制备NO并验证其还原性.
用如图示装置制备NO并验证其还原性.
 .
.