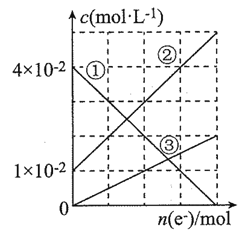题目内容
【题目】某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
(实验原理)2KMnO4 + 5H2C2O4 + 3H2SO4=K2SO4 + 2MnSO4 + 10CO2↑ + 8H2O
(实验内容及记录)
实验编号 | 室温下,试管中所加试剂及其用量/mL | 室温下溶液颜色褪至无色所需时间/min | |||
0.6 mol/L H2C2O4溶液 | H2O | 3 mol/L 稀硫酸 | 0.05mol/L KMnO4溶液 | ||
1 | 3.0 | 2.0 | 2.0 | 3.0 | 1.5 |
2 | 2.0 | 3.0 | 2.0 | 3.0 | 2.7 |
3 | 1.0 | 4.0 | 2.0 | 3.0 | 3.9 |
请回答:
(1)根据上表中的实验数据,可以得到的结论是__________________。
(2)该小组同学根据经验绘制了n(Mn2+)随时间变化趋势的示意图,如图1所示。但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+) 随时间变化的趋势应如图2所示。该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究。
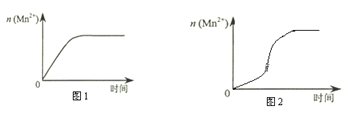
该小组同学提出的假设是___________________________________________________。
(3)测血钙的含量时,进行如下实验:
①可将4mL血液用蒸馏水稀释后,向其中加入足量草酸铵(NH4)2C2O4晶体,反应生成CaC2O4沉淀,将沉淀用稀硫酸处理得H2C2O4溶液。
②将①得到的H2C2O4溶液,再用酸性KMnO4溶液滴定,氧化产物为CO2,还原产物为Mn2+。
③终点时用去20mL l.0×l0-4mol/L的KMnO4溶液。
Ⅰ、滴定终点的现象是_________________________________。
Ⅱ、下列操作会导致测定结果偏低的是______。
A.锥形瓶用待测草酸溶液润洗
B.滴定过程中,锥形瓶摇荡得太剧烈,锥形瓶内有液滴溅出
C.酸式滴定管尖嘴部分在滴定前没有气泡,滴定终点时发现气泡
D.达到滴定终点时,仰视读数
Ⅲ、计算:血液中含钙离子的浓度为______mol/L。
【答案】其他条件相同时,增大H2C2O4浓度(或反应物浓度),反应速率增大 生成物中的MnSO4为该反应的催化剂(或Mn2+对该反应有催化作用) 当滴入最后一滴酸性KMnO4溶液后溶液由无色变为浅紫色,且半分钟内不褪色 BC 1.25×10-3
【解析】
(1)根据表中数据,溶液的总体积不变,取用草酸的体积不同,导致草酸的浓度不同,草酸的浓度越大,溶液褪色的时间越短,则结论为其他条件相同时,增大H2C2O4浓度(或反应物浓度),反应速率增大;
(2)根据图2,反应开始时,n(Mn2+)逐渐增大,在某一时刻n(Mn2+)瞬间增大,反应速率加快,则生成物中的MnSO4为该反应的催化剂(或Mn2+对该反应有催化作用);
(3)Ⅰ、实验是用高锰酸钾滴定草酸,终点时,高锰酸钾多滴加一滴,溶液显紫红色,则滴定终点为当滴入最后一滴酸性KMnO4溶液后溶液由无色变为浅紫色,且半分钟内不褪色;
Ⅱ、A.锥形瓶用待测草酸溶液润洗,导致草酸的物质的量增大,使用高锰酸钾的量增多,计算草酸的浓度偏高,与题意不符,A错误;
B.滴定过程中,锥形瓶摇荡得太剧烈,锥形瓶内有液滴溅出,导致草酸的物质的量减小,使用高锰酸钾的量减小,计算草酸的浓度偏低,符合题意,B正确;
C.酸式滴定管尖嘴部分在滴定前没有气泡,滴定终点时发现气泡,导致读取高锰酸钾溶液的体积偏小,计算草酸的浓度偏低,符合题意,C正确;
D.达到滴定终点时,仰视读数,导致读取高锰酸钾溶液的体积偏大,计算草酸的浓度偏高,与题意不符,D错误;
答案为BC;
Ⅲ、根据方程式可知2KMnO4~5H2C2O4,则0.02L×l.0×l0-4mol/L×5=2n(H2C2O4)=2n(CaC2O4),n(H2C2O4)=n(CaC2O4)=5.0×l0-6mol,则c(Ca2+)=5.0×l0-6mol÷0.004L=1.25×10-3 mol/L。

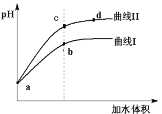
【题目】已知T ℃时两种弱酸的电离平衡常数如下表。将pH和体积均相同的两种酸溶液M、N分别稀释,其pH随加水体积的变化如图所示。下列叙述不正确的是
弱酸 | HNO2 | CH3COOH |
电离平衡常数 | 5.0×10-4 | 1.7×10-5 |
A.曲线Ⅰ代表CH3COOH溶液
B.M、N两溶液分别与NaOH恰好中和后,溶液中n(Na+)相同
C.溶液中水的电离程度:b点<c点
D.从c点到d点,溶液中 保持不变(其中HA、A-分别代表相应的酸和酸根离子)
保持不变(其中HA、A-分别代表相应的酸和酸根离子)
【题目】下表是25℃时弱酸的电离平衡常数,下列说法正确的是
CH3COOH | HClO | H2CO3 |
Ka=1.8×10—5 | Ka=3.0×10—8 | Ka1=4.1×10—7 Ka2=5.6×10—11 |
A.根据表中数据可知,相同浓度CH3COONa和NaClO的混合溶液中,各种离子浓度的大小关系是:c(Na+)>c(ClO﹣)>c(CH3COO﹣)>c(OH﹣)>c(H+)
B.根据表中数据可知,次氯酸钠溶液中通入少量CO2的离子方程式为:2ClO﹣+CO2+H2O=CO32﹣+2HClO
C.向0.1mol·L-1CH3COOH溶液中加入少量水,溶液中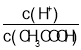 减小
减小
D.室温下,将碳酸钠溶液加热至70℃,溶液的中的OH—数目增多
【题目】苯甲醛(微溶于水、易溶于有机溶剂,密度约等于水的密度)在碱性条件下发生歧化反应可以制备苯甲酸和苯甲醇(在水中溶解度不大,易溶于有机溶剂,密度约等于水的密度)。反应原理如下:
2C6H5CHO+NaOH→C6H5CH2OH+C6H5COONa
C6H5COONa+HCl→C6H5COOH+NaCl
相关物质物理性质如表:
苯甲醛 | 苯甲醇 | 苯甲酸. | 苯 | |
沸点/℃ | 178 | 205 | 249 | 80 |
熔点/℃ | 26 | -15 | 122 | 5.5 |
苯甲酸在水中的溶解 | ||
17℃ | 25℃ | 100℃ |
0.21g | 0.34g | 5.9g |
实验流程如下:

(1)操作①需连续加热1小时(如图1),其中加热固定装置未画出。

仪器A的名称为___,若将仪器B改为图2中的仪器C,效果不如B,请说明原因___。
(2)操作②有关分液漏斗的使用不正确的是___(填字母)。
A.分液漏斗在使用之前必须检查是否漏水
B.分液漏斗内的液体不能过多,否则不利于振荡
C.充分振荡后将分液漏斗置于铁架台上静置,分层后立即打开旋塞进行分液
D.分液时待下层液体放完后立即关闭旋塞,换一个烧杯再打开旋塞使上层液体流下
(3)操作③是用沸水浴加热蒸馏,再进行操作④(如图2),收集___℃的馏分。图2中有一处明显错误,正确的应改为___。
(4)抽滤时(如图3)烧杯中苯甲酸晶体转入布氏漏斗时,杯壁上还粘有少量晶体;用___冲洗杯壁上残留的晶体。抽滤完成后用少量冰水对晶体进行洗涤,洗涤前应先___。
(5)用电子天平准确称取0.2440g苯甲酸于锥形瓶中加100mL蒸馏水溶解(必要时可以加热),再用0.1000mol·L-1的标准氢氧化钠溶液滴定,共消耗标准氢氧化钠溶液19.20mL,苯甲酸的纯度为___%。